Anno scolastico 1998-99
Corso B Scuola Media N° 3 Olbia

Anno scolastico 1998-99 Corso B Scuola Media N° 3 Olbia |

|
S'omine e s'abba
La cumpusizioni chimica di l'ea
Illu laboratoriu, cu' un sistema cumplicatu, chi si chjama "elettrolisi", fendi passà la correnti elettrica ill'ea distillata, si po' scumpunì l'ea in li dui sustanzi chi la cumpunini: l'idrogenu e l'ossignenu. Una 'olta scumposta l'ea cu' "l'elettrolisi" vidimu chi l'idrogenu è lu doppiu di l'ossigenu. Diffatti la "formula" chimica di l'ea è H20.
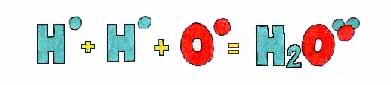

Illa molecola di l'ea, l'idrogenu si miscia a l'ossigenu palchì un atomu di l'ossigenu s'attira l'elettròni senza parò riscì a staccallu da l'idrogenu.
L'idrogenu di una molecola d'ea tendi a liassi cu' l'ossigenu di un'alta molecola d'ea, chistu di dici "legami a idrogeno" o "ponti a idrogeno".
Chistu fattu lassa a l'ea li so' galitai fisici e lu so' calori specificiu: difatti si scaldi e s'infrisca a poc'a pocu.
Iscrittu in gadduresu dai
Fabrizio Demontis
Francesco Demontis