


|
|


|
NUOVI
FANS E VIE DI SOMMINISTRAZIONE ALTERNATIVE
A.F. SABATO, C. PISANELLI*, M.G. CELESTE**, G. SERAFINI***, A. GATTI^
Università degli Studi di Roma "Tor Vergata" Cattedra di
Anestesia Generale e Speciale Odontostomatologica
*Servizio di Farmacia - Azienda Ospedaliera San Filippo Neri
- Roma
**Servizio di Farmacia ASL RM/C Ospedale S. Eugenio - Roma
***Università degli Studi di Roma "Tor Vergata"
Scuola di Specializzazione in Anestesia e Rianimazione (Dir. Prof. G.
Leonardis)
^Università degli Studi di Roma "Tor Vergata" Cattedra di
Anestesia e Rianimazione (Dir. Prof. G. Leonardis)
Nella graduatoria dei
farmaci più prescritti e più impiegati in tutti i settori della pratica
clinica, la classe farmacologica dei FANS occupa attualmente una posizione di
tutto rilievo oltre a vantare la maggiore anzianità nella storia dei farmaci di
sintesi (salicilato di sodio 1875, paracetamolo 1878).
Essa è costituita da una
congerie di composti dissimili tra loro sia dal punto di vista chimico che
farmacologico.
La triade
ANALGESICO-ANTINFIAMMATORO-ANTIPIRETICO che ne generalizza le proprietà
farmacologiche, giustifica tra l'altro
il vasto impiego in quasi tutte le condizioni cliniche.
Negli ultimi dieci anni i
notevoli sforzi della ricerca in questo importante settore (spesso coronati da
ragguardevoli successi) si sono articolati in tre filoni :
1 - il filone chimico ove si
è tentata la sintesi di nuovi composti più potenti e con effetti collaterali
attenuati rispetto alle molecole già esistenti
2 - il filone
tecnico-farmaceutico volto alla continua ricerca di forme e formulazioni
farmaceutiche contraddistinte da una migliore cinetica di assorbimento di
molecole già utilizzate da tempo nella pratica clinica
3 - il filone clinico che si
è proposto di valutare in pratica le differenze tra i vari termini del gruppo
sia in termini di profilo farmacoterapeutico che di elettività d'organo o di
tessuto come corollario di accurati studi farmacocinetici.
E' auspicabile che tutto ciò
possa portare ad un più preciso e razionale aggiornamento della classificazione clinica dei FANS basata
sulla pratica terapeutica e non solamente sulla suggestiva letteratura
propagandistica generando criteri di
scelta più razionali e, cosa di non poco conta, ad una valutazione COSTO\EFFICACIA e COSTO\BENEFICIO ormai implicitamente imposta dalle leggi finanziarie in materia
di sanità per farmaci, come i FANS, di ampia utilizzazione.
Uno degli aspetti che
caratterizzato i FANS da altri farmaci utilizzati nel trattamento del dolore è
la possibilità di somministrazioni per periodi di tempo molto prolungati nelle
sindromi nelle quali l'elaborazione degli impulsi nocicettivi non costituisce
più una risposta ad uno stimolo dannoso ma diviene responsabile di effetti
distruttivi e disgreganti dell'integrità fisica e psichica dell'individuo che
ne è affetto.
Come in tutte le
somministrazioni croniche subentrano quindi problemi quali effetti collaterali,
tossicologia spesso espressa con vere e proprie lesioni anatomopatologiche di
organi, diminuzuione di efficacia e ridotta compliance.
I FANS dell'ultima generazione hanno dato nella
sperimentazione clinica promettenti possibilità di minimizzare alcuni qi questi
inconvenienti. Particolarmente interessante si è rivelata la selettività
farmacodinamica delle molecole studiate più recentemente.
Il recente chiarimento delle
differenze biochimiche e dei conseguenti ruoli fisiologici delle due unità
isoenzimatiche delle ciclossigenasi (ciclossigenasi I o COX1 e ciclossigenasi II o COX2)[1]
hanno orientato la ricerca verso la sintesi di composti che presentassero una
maggiore attività inibitoria enzimatica nei confronti della ciclossigenasi II.
La COX1 ha il compito di
controllare omeostaticamente la produzione fisiologica di prostaglandine. In
seguito a stimoli fisiologici di varia natura la COX1 catalizza la biosintesi
del trombossano A2 nelle
piastrine, della prostaglandina I2 nell'endotelio vasale e nella
mucosa dello stomaco ed infine della prostaglandina E2 nel rene ed
in altri siti.
La COX2 viene invece
biosintetizzata per induzione a seguito di stimoli infiammatori
contemporaneamente alla migrazione nel tessuto infiammato di macrofagi
produttori di enzimi proteasici e di altre cellule produttrici di altri
mediatori della infiammazione tra cui tra cui le prostaglandine S la cui
produzione è catalizzata dalla COX2.
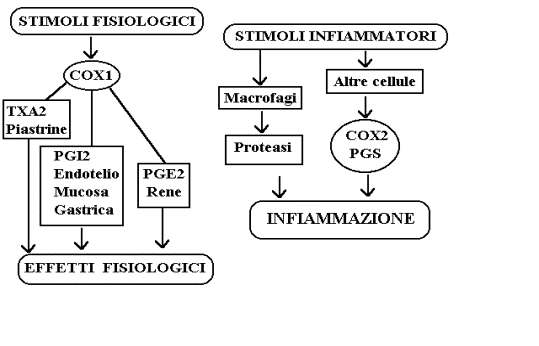
Questa fondamentale differenza tra le due unità isoenzimatiche
ha anche chiarito che gran parte della tossicologia dei FANS non selettivi
come la gastrolesività e la nefrotossicità è dovuta alla inibizione della COX1
mentre la attività terapeutica è da ascriversi alla sola interazione con la
COX2.
Ovviamente i FANS classici interagiscono in misura
diversa con i due isoenzimi ed è stato visto che l'ibuprofen presenta la minima attività anti-COX1 mentre il piroxicam
tra quelli più attivi sulla COX1; ciò si accorda bene con i dati
esistenti sugli effetti collaterali delle due molecole.
Gli studi epidemiologici
hanno confermato che l'intensità e la diffusione
dei tipici effetti collaterali dei FANS sono direttamente proporzionali
al rapporto tra inibizione della COX2 ed inibizione della COX1 (COX2\COX1). I
dati si riferiscono in particolar modo al sanguinamento gastrico e alla
riduzione della circolazione intrarenale con le prevedibili conseguenze.
Tra i nuovi composti dotati
di attività inibitrice selettiva nei confronti della coclossigenasi II
particolarmente interessante è risultato il MELOXICAM[2][3][4] testato su oltre cinquemila pazienti.
In studi comparativi con
piroxicam, diclofenac e naprossene hanno mostrato
una netta diminuzione del danneggiamento gastrico e della
tossicità in generale. Pertanto il principio attivo presenta un netto
miglioramento del rapporto RISCHIO/BENEFICIO[5][6][7].
Altri promettenti FANS che si contraddistinguono sia per la ridotta
gastrolesività e per la diminuzione della temuta tossicologia renale[8] che per le peculiarità fasrmacocinetiche che
consentono somministrazioni prolungate sono :
lo ZALTOPROFENE[9]
e l'ACECLOFENAC per uso sia orale
che iniettabile[10], il LOXOPROFENE
SODICO[11] e l'AMPIROXICAM[22], quest'ultimo un profarmaco del
piroxicam del quale non presenta
alcuna gastrolesività.
L'aceclofenac è un derivato
del diclofenac attivo alla dose orale di 100 mg e sperimentato anche per via
parenterale alla dose di 150 mg[12]. In una studio multicentrico
comparativo[13] effettuato su pazienti affetti da lombalgia acuta ha
mostrato proprietà antinfiammatorie ed analgesiche equivalenti a quelle del
diclofenac ma con una tollerabilità superiore. Inizialmente sono stati
somministrati 150 mg per via intramuscolare nei primi due giorni e
successivamente compresse da 100 mg tre volte al dì per cinque giorni in
confronto a 75 mg di diclofenac sodico per via intramuscolare nei primi due
giorni e due compresse al di da 50 mg nei cinque giorni successivi. Otto ore
dopo la prima somministrazione parenterale la diminuzione dell'intensità del
dolore si è mostrata più pronunciata nel gruppo a cui è stato somministrato
l'aceclofenac. Altre valutazioni effettuate successivamente sono pure a favore dell'aceclofenac.
Un solo paziente del gruppo a cui è stato somministrato aceclofenac e ben
cinque pazienti del gruppo del diclofenac hanno dovuto interromoere il
trattamento a causa degli effetti collaterali.
Il lornoxicam è un derivato
clorurato del tenoxicam del quale conserverebbe la medesima potenza antalgica e
dotato in più di una più capillare diffusività tissutale.[15]
A livelli ancora puramente
sperimentali si stà indagando sulle attività antinocicettive del BROMFENAC e DEXPEMEDOLAC[16] per somministrazione intratecale ed
intracerebroventricolare nel ratto, come pure il composto
(b)-N-N-dimetilcarbamoilmetil-2[7(2-metil-5H-[1]-Benzopirano[2,3-B]-Piridil)]-Propionato
o Y-23023[17]
ed altri ancora[18][19][20].
Uno studio clinico condotto
con lo zaltoprofene nel trattamento del dolore post-operatorio[21]
ha mostrato una diminuzione percentuale degli effetti gastrolesivi rispetto ad
altri FANS.
Dopo il successo clinico
della somministrazione del piroxicam sotto forma di liofilizzato incluso in una
matrice di gelatina e mannitolo fatta assorbire attraverso la rete vasale del
pavimento orale che convogliando il farmaco direttamente nella vena cava superiore
evitando il circolo portale e quindi il metabolismo epatico oltre a limitare
eventuali danneggiamenti esofagei ed espletando analgesia in tempi brevissimi
in ogni tipo di dolore[26][27][28], si sono succeduti altri studi volti alla
quantizzazione del potere analgesico in
clinica di FANS di comprovata efficacia adottando nuove vie di
somministrazione.
La somministrazione di
paracetamolo per via endovenosa sotto forma di profarmaco, il PROPACETAMOLO produce elevati effetti
analgesici in ogni tipo di dolore[29][30][31] essendo un farmaco di cui è stata
recentemente ribadita la componente analgesica centrale [32] probabilmente
dovuta alla preferenziale inibizione della ciclossigenasi cerebrale e spinale
piuttosto che di quella dei tessuti periferici, forse supportata anche da una
distribuzione nel liquido cerebrospinale in seguito a somministrazione
endovenosa[33]. Il potere analgesico dipenderebbe anche dal metodo di
somministrazione[34].
La somministrazione
post-operatoria di ketoprofene con microinfusore[35] ha ridotto in modo
significativo l'entità ed i tempi di richiesta di buprenorfina nelle
ventiquattro ore successive all'intervento chirurgico. Il dato più rilevante è
quello concernente il tempo di richiesta dell'oppioide, dal quale si può dedurre
l'intervallo libero dal dolore. E' stata altresì dimostrata l'efficacia anche
pre- e intra-operatoria della somministrazione del ketoprofene in micropompa
nel controllo del dolore post-operatorio[35][36] dove risulterebbe non una
diminuzione complessiva del consumo di altri analgesici ma semplicemente ne
ritarderebbe il tempo di richiesta.
Infine le attuali
sperimentazioni riguardano vie alternative al fine di evitare il contatto
diretto con la mucosa gastrica; tra queste sono da citare l'inclusione dei FANS
in matrici fosfolipidiche zwitterioniche[37] e la somministrazione in sistemi
transdermici del flurbiprofen date le sue caratteristiche farmacocinetiche
favorevoli ad un tale tipo di assorbimento[38].
In tutte le patologie
algiche i FANS vengono somministrati in quanto la riduzione della biosintesi
delle prostaglandine da essi attuata a più livelli, comporta sempre una
significativa riduzione del dolore e del consumo di analgesici appartenenti ad
altre categorie farmacologiche; a ciò si affianca un netto miglioramento di
sintomi spesso correlati ad alcune forme di dolore (febbre, flogosi, nausea
ecc.).
Data l'importanza clinica di
questi farmaci, l'obiettivo principale della ricerca non è quello di aumentare
la potenza analgesica dei FANS ma di migliorarne la tollerabilità sistemica
annullando o riducendo gli effetti collaterali che si verificano nelle
somministrazioni croniche, di ottenere
un più rapido esordio dell'effetto analgesico nelle somministrazioni acute ed
infine di aumentare la compliance dei pazienti.
Attualmente si cerca di raggiungere
questi obiettivi o con la sintesi di composti ad azione selettiva o mettendo a
punto vie di somministrazione alternative valutando poi in entrambi i casi la
tollerabilità e la rapidità di efficacia con metodologie standardizzate.
B
I B L I O G R A F I A
[1] - Crofford L. "Improved non-steroid anti-inflammatory drugs;
COX-2 enzyme inhibitors"
William Harvey Press/Kluver; London
-1996-
[2]
- Huskisson E.C. ; Naries H. ; Bluhmki E. "Efficacy and
tolerability of meloxicam, a new NSAIS, in daily oral doses
of 15, 30
and 60 mg in comparison to 20 mg piroxicam in pa-
tients
with reumatoid arthritis"
Scand J Rheumatol -1994- (Suppl
98):Abstract 115
[3]
- Lund B. ; Distel M. ; Bluhmki E. "A
double bind placebo-
-controlled study of three different doses of meloxicam in
patients
with osteoarthritis of the knee"
Scand J Rheumatol -1994- (Suppl
98):Abstract 117
[4]
- Linden B. ; Distel M. ; Bluhmki E. "Double-blind,
randomized
comparison
of meloxicam and piroxicam in patients with
osteoarthritis of the hip"
Scand J Rheumatol -1994- (Suppl 98);
Abstract 192.
[5]
- Lamgman M.J. ; Well J. ; "Risks of
bleeding peptic ulcer
associated with individual non-steroidal anti-infiammatory
drugs"
Lancet -1994- 343: 1075-1078.
[6]
- Rodriguez L.A.G. ; Hershel J. "Risks
of upper gastro-
intestinal bleeding and perforation associated with
individual non-steroideal anti-inflammatory drugs"
[7] - Mitchell J.A. ; Akarasereemont P. ;
Thiemermann C. ;
Flower
C. , Vane J.R. "Selectivity of non-steroidal
anti-inflammatory drugs as inhibitors of constitutive and
inducible
cycloxygenase"
Proc Nati Acad Sci -1994-
90:11.693-11697.
[8]
- Ekelof N.P. ; Olsen N.V. ; Ording H.
"Renal side-effects in per- and postoperative pain treatment with
non-steroidal anti-inflammatory drugs"
Ugeskr-Laeg -1995- 157\19:2703-2707.
[9] - Rabasseda X. ; Mealy N. ; Hopkins S.J.
"Zaltoprofen : a new NSAID
less likely to induce gastric
mucosal
lesions"
[10]
- Honorato J. ; "Dose-analgesic
response study and
aceclofenac plasma levels in humans"
Curr Ther Res -1990- 47:605-11
[11]-
Kawano S. ; Tsuji S. ; Hayashi N. ; Takey Y. ; Nagano K.;
Fusamoto H. ; Kamada T.
"Effects of loxoprofen sodium, a newly synthetized non-
-steroidal anti-inflammatory drug, and indomethacin on
gastric
mucosal haemodynamics in the human"
J Gastroenterol-Hepatol
-1995- 10\1:81-85.
[12]-
Torrent A.P. "Dose-response study of
the analgesic activity
of
aceclofenac in odontalgia following extraction of the
third
molar"
Drug Invest -1990- 2:132-5.
[13] - Agrifoglio E. ; Benvenuti M. ; Gatto P. ;
Cherubino P.
Marinoni E.C. ; Fontana A. ; Peretti G.
"Aceclofenac : a new NSAID in
the treatment of acute
lumbago.
Multicentre single blind study vs diclofenac"
Acta Ther 20/1-2(33-45) -1994-
[14]-
Desjardins P.J. "Analgesic efficacy
of lornoxicam in dental
impaction
pain"
Clin Pharmacol Ther -1992- 51:123.
[15]-
"Lornoxicam.Safem registered"
Drugs-Future -1995- 20\b:835-836
Journal Artucle
[16]- Walter T.L. ; Chau T.T.
"Antinociceptive activities of non-steroidal
antiinflammatory drugs (NSAID) following intracerebroventricular
(i.c.v.) and intratecal(i.t.)
administration in mice"
Inflamm Res 44\suppl 2
(s133-s134)-1995-
[17]-
Iwahisa Y. ; Yasunaga Y. ; Ochi H. ; Matsuura M. ;
Imayoshi
T. ; Terasawa M. :
"Anaslgesic and antinflammatory effect of
(b)-N-N-dimetilcarbamoilmetil-2[7(2-metil-5H-[1]-
Benzopirano[2,3-B]-Piridil)]-Propionato ( Y-23023), a non-steroidal
antiinflammatory drug"
[18]-
Rang H.P. ; Urban L.
"New molecules in analgesia"
Br J Anaesth -1995- 75\2
:145-6.
[19]-Satyabarayana K. ;
Rao M.N.A.
Synthesis of 4-[5-(substituted
aryl)-4,5-dihydro-1H-pyrazol
-3-yl]-3-phenyl-sydnones as antiinflammatory, antiarthritic
and
analgesic agents"
Eur J Med Chem
30\7-8:641-645
[20]-
Birch P.J.
"Clinical relevance of receptor pharmacology in the
nociceptive pathway"
Pain Rev
-1995- 2\1:13-27
[21]-
Monden M.
"Clinical study of zaltoprofen, a nonsteroidal anti-
inflammatory drug in postoperative pains"
JPN Pharmacol Ther -1995-
[22]- Rabadessa X. ;
Hopkins S.J.
"Ampiroxicam : a prodrud of piroxicam devoid
of gastro-
intestinal toxicity"
Drugs-today -1994- 30\7 (557-563)
[23]-
Erol D.D. ; Demirdamar R.;
Analgesic
and antinflammatory activity screening of
6-acyl-3-piperidinomethyl-2(3h)-benzoxazolone derivatives
Farmaco -1994- 49\10:663-6.
[24]- Savini L. ; Massarelli P. ; Chiasserini L. Pellerano
C.
Bruni G.
"New 1-[quiinolyl(4)-1,2,3-triazoles : synthesis and
evaluation of antiinflammatory and analgesic properties"
Farmaco -1994- 49\10:633-39.
[25]- Ronca F. ; Palmieri L. ; Ronca G.
"Effetto della formulazione e della voa di somministrazione
sulla velocità di assorbimento del
piroxicam"
Basi Taz Ter -1994- vol XXIV:1-6
[26]-
Consoli G. ; Covelli M. ; Di Matteo L. ; Marcolongo G.
Tirri
G. ; La Montagna G. e Pipitone V.
"Piroxicam compresse sublinguali a rapida
dissoluzione
versus naprossene nel trattamento
dell'osteoartrosi
riacutizzata"
Minerva Medica -1994- 85(3):89-96.
[27]- Franchin F. ; Oriano C. ; Cuomo A. ; Pipino E.
"Valutazione dell'efficacia clinica del
piroxicam
compresse sublinguali a rapida
dissoluzione nelle
affezioni muscolo-scheletriche acute"
Incontri Di ortopedia 7(1):43-8.
[28]- Montecucco C. ; Caporali R. ; Ronchetti A. ;
Rossi S. ;
Comaschi E. ;
"Il piroxicam FDDF per via
sublinguale nel trattamento
dell'artrite reumatoide"
Minerva
Med-1994-85:633-8.
[29]- Stipon J.P.; Le
Bihan Y.; De RotalierP. :
"Evaluation of analgesic action of
propacetamol in
patients
with acute ENT pain"
Sem
Hop Paris-1983-59(39):2725-8.
[30]-
Van Acken H. ; et coll
"Analgesic action and tolerance of
propacetamol versus
morphine
and placebo after extractionof an impacted
3rd
molar tooth"
Seventh Wordl Congress on Pain,
Paris,-August-1993-
[31]-
Delacroix P.
"Analgesic action and tolerance of propacetamol in cancer
pain"
Rev. Fr. Gynecol. Obstet-1983-78(6):487-9.
[32]- Pilletta P. et
coll
"Central analgesic effect of paracetamol"
Clin Pharmacol Ther-1991-(49),4:350-4.
[33]-
Bannwarth et coll
"Plasma and cerebrospinal fluid concentrations of
paracetamol after a single intravenous dose of
propacetamol"
Br J
Clin Pharmacol-1992-17-20.
[34]- Luthy C.S. et coll.
"Effect of
administration method of propacetamol on
its
analgesic action"
Clin Pharmacol Ther-1993-(53),2,171,28
[35]- Forastiere E.M.A. ; Belcastro F. ; Costanzo L.
; Piastra M.
Diamanti P. e Greco R.
"Effetti della somministrazione pre- intra e
post-operatoria
dei FANS nel controllo del dolore
post-operatorio"
Pathos-1995-Vol 2(4):182-5.
[36]-
Katz J.;
"Preoperative analgesia for post-operative pain"
ancet-1993-342:65-6.
[37]-
Lichtenberger-L.M.; Wang Z.M.; Romero J.J.; Ulloa C.;
Perez J.C.; Giraud M.N.; Barreto J.C.
"Non steroidal anti-inflammatory drugs (NSAIDs) associate
with zwitterioni
phospholipids : insight into the mechanism
reversal
of NSAID -induced gastrointestinal injury".
Nat Med -1995- 1\2:154-8.
[38]-
Davies N.M.
"Clinical pharmacokinetic of flurbiprofen and its
enantiomers"
Clin
Pharmacokinet -1995- 28\2:100-14.
 ©Copyright Progetto Salute
©Copyright Progetto Salute