


|
|


|
IL DOLORE MIOFASCIALE
FISIOPATOLOGIA, DIAGNOSI DIFFERENZIALE E TERAPIA
G. SERAFINI* - A. F. SABATO
Università degli Studi di Roma Tor Vergata
*Scuola di Specializzazione in Anestesia e Rianimazione (Dir. Prof. G. Leonardis)
Cattedra di Anestesia Generale e Speciale
Odontostomatologica
SOMMARIO
A. Introduzione
1. Fibre del gruppo III (Tipo A)
2. Fibre del gruppo IV (Tipo C amieliniche)
C. Forme miste
III. INTRODUZIONE ALLA TERAPIA
A. Premessa
IV. TERAPIA
A. Obiettivi
a) Attiva
(1) Ginnastica posturale Mezieres
b) Passiva
(b) T.E.N.S.
(c) Agopuntura-Elettroagopuntura
(e) Massoterapia
(2) Farmacologica
(b) Mesoterapia
3. Terapia farmacologica sistemica
V. CONCLUSIONI
VI. BIBLIOGRAFIA
Riassunto
Il dolore miofasciale primitivo essenziale è una diagnosi relativamente poco conosciuta che evoca l’immagine di un dolore vago, generalizzato, associato a disfunzione. Tuttavia, nonostante una storia di teorie controverse e di una confusa terminologia, il suo inquadramento fisiopatologico e diagnostico sta diventando clinicamente utile nella classificazione di un’ampia varietà di condizioni dolorose somatiche.
Uno dei criteri, comunque, ritenuto più utile in fase differenziale è l’inquadramento in forme cliniche generalizzate, loco-regionali e miste.
I metodi di trattamento del dolore miofasciale ( nelle sue varie espressioni cliniche e relativi sinonimi) sono numerosi come i terapisti che si cimentano ad affrontarlo. Quadro clinico d’intersezione ( e talvolta di contrapposizione) tra varie specialità, l’apparente varietà di approcci terapeutici possibili denuncia la sostanziale fragilità di ogni specifica modalità, evidenziandone, al di là di ogni opinione, una carenza di provata efficacia.
Come molti interventi in medicina in generale e in algologia in particolare, la strategia terapeutica proposta in questo scritto non è stata oggetto di un rigoroso studio controllato. Si basa, comunque, sull’esperienza elaborata nel nostro ambulatorio di terapia del dolore, orientata sulle linee guida del Dipartimento di Medicina Fisica e Riabilitativa della Mayo Clinic di Rochester.
Parole chiave: dolore muscolo-scheletrico, dolore muscolare, dolore miofasciale, fisipatologia, diagnosi differenziale, terapia
Summary
Essential primitive myofascial pain (EPMP) diagnosis is relatively little known. This painful state is associated to the idea of a vague, generalized and dysfunctional pain. Nevertheless, its diagnosis and the knowledge of underlying pathophysiology is becoming clinically useful in chronic muscle pain classification.
In fact, first step is chronic muscle pain arrangement in generalized, loco-regional and mixed clinical features. The methods of treating EPMP (and its synonyms) are as numerous as the clinicians who attempt to treat it. The number of approaches is evidence of lack of proven efficacy for any specific modality. As with many interventions in medicine in general and in pain medicine in particular, the treatment approach outlined herein has not been subjected to a rigorous controlled study. However, drug, multidrug and drug alternatives treatments are shown, based on the cumulative experience of multiple clinicians in our pain clinic, under guide lines of the Department of Physical Medicine and Rehabilitation at the Mayo Clinic in Rochester.
Key words: musculoskeletal pain, muscle pain, myofascial pain, pathophysiology, differential diagnosis, therapy.
La ricerca clinica e sperimentale sul dolore presenta ancora molti punti oscuri, la maggior parte però riguarda soprattutto il dolore di origine muscolare, per es. la dolenzia muscolare, lo spasmo, i tender points e i trigger points. Inoltre la differenza tra questo tipo di nocicezione e quella derivante dai tessuti cutanei o viscerali presenta il problema della perfusione/ischemia anche durante un lavoro muscolare normale.
Tutto ciò è complicato dal fatto che il muscolo scheletrico è un target di riflessi (es. simpatici e fusimotori) che possono provocare modificazioni nell'apporto di sangue e del tono muscolare anche durante condizioni di riposo. Infine il muscolo scheletrico è la tavolozza degli stati emozionali soprattutto nei mammiferi superiori e di conseguenza modificazioni psichiche del tono muscolare possono portare a modificazioni del tono muscolare e di conseguenza a possibili situazioni di dolore.
Comunque lo studio sul dolore muscolare ha subito negli ultimi anni notevoli progressi, , anche se non sono del tutto chiariti alcuni meccanismi di fisiopatologia , come ad esempio il dolore nelle miositi.
Stacey nel 1969 dimostrò che oltre i recettori dello stiramento muscolare (stretch receptors), il 75% dell'innervazione sensitiva del muscolo veniva supportata da terminazioni nervose libere a livello della fascia muscolare, a livello intramuscolare, a livello della parete vascolare nei tendini, e che queste terminazioni erano di tipo mielinizzato (gruppo III) e amieliniche (Gruppo IV) [Tab.VII]. Dopo aver perso la guaina mielinica le terminazioni libere potevano percorrere tratti lunghi anche 1 mm come assoni nudi e innervare campi muscolari grandi in un range compreso tra 25-200 m.
Gli impulsi dolorifici vengono veicolati da fibre afferenti amieliniche e finemente mieliniche a lenta conduzione.
Le terminazioni recettive connesse a queste fibre sono del tipo non capsulato e pertanto definite "terminazioni nervose libere " Recentemente Studi sul tendine di Achille del gatto hanno evidenziato che non sono completamente "libere" ma parzialmente coperte da processi delle cellule di Scwann .
Le proprieta' funzionali di queste terminazioni sono in relazione dalla loro morfologia.
Esistono recettori che rispondono solo alla forza meccanica della contrazione e recettori, di particolare interesse clinico, che sembrano essere nocicettori , attivati dalle contrazioni muscolari soltanto se l'irrorazione sanguigna viene interrotta.
Questo tipo di recettore sarebbe responsabile del dolore che compare nella claudicatio intermittens. Anche questo tipo di dolore ischemico e' condotto attraverso vie afferenti amieliniche.
I nocicettori muscolari pur rispondendo a vari stimoli dolorifici meccanici e chimici non possono definirsi polimodali.
Il concetto di polimodalita' quando applicato ai recettori muscolari implica che tutte le terminazioni nervose libere terminino sotto un'unica popolazione funzionale che ha una certa variabilita biologica nella soglia meccanica e nella sensibilita' chimica. Cosi' scariche a basse frequenze di quelle popolazioni codificano la presenza di uno stimolo innocuo e scariche ad alte frequenze codificano stimoli nocicettivi.
Le fibre afferenti del gruppo III possono essere eccitate da stimoli meccanici applicati direttamente sul muscolo o indirettamente sui tendini, ma non sono sensibili allo stiramento di per se o all'ischemia se il muscolo si trova in posizione di riposo. Dato che queste fibre afferenti del gruppo III sono attivate da stimoli soglia il cui range va dalla pressione lieve a quella molto forte, per questa ragione furono chiamate da Paintal "terminazioni nervose pressione-dolore".
Mense e Stahnke nel 1977 dimostrarono che oltre il 70% di queste fibre A erano eccitate dalla somministrazione intrarteriosa muscolare di bradichinina, 5HT, His o KCl. Queste fibre erano inoltre eccitate da stimoli caldi applicati sul corpo muscolare o dall'iniezione di soluzione ipertonica di cloruro di sodio all'interno del muscolo.
Più recentemente Mense e Stahnke (1983) notarono che una parte di fibre afferenti A rispondevano allo stiramento e alla contrazione muscolare, ma che mostravano una risposta di contrazione ridotta in presenza di ischemia. Gli autori concludevano che gran parte delle fibre del gruppo III fossero più facilmente attivabili durante l'esercizio rispetto alle fibre afferenti del gruppo IV e che il loro ruolo poteva essere più ergorecettivo che nocicettivo.
In generale sono similari a quelle del gruppo III solo che la loro soglia allo stimolo meccanico è più alta (5-50 g di pressione), i loro campi recettoriali sono piccole aree di muscolo e di tendine, l'adattamento è lento e poche fibre rispondono allo stiramento e nessuna alla contrazione.
Il gruppo di Mense trovò che le fibre amieliniche erano attivate come le A da sostanze irritanti come la bradichinina, 5HT, His o KCl iniettate per via intrarteriosa muscolare. Dosi ripetute di bradichinina producevano sempre la stessa risposta, al contrario dosi ripetute di 5HT producevano tachifilassi, questo esperimento fece supporre che le diverse sostanze agissero in differenti siti di membrana. La PGE2 e la 5HT agirebbero soprattutto come sostanze sensibilizzanti nei riguardi della bradichinina.
Ogni sostanza irritante inoltre attiverebbe gli afferenti amielinici in modo distinto, e ciò si può rivelare o attraverso un allungamento dell'onset o della durata o della frequenza di scarica.
Molte di queste unità nervose sono di tipo polimodale come quelle riscontrabili a livello cutaneo. Il gruppo di Kniffki (1978) ha suddiviso questo gruppo IV in 3 sottogruppi:
a) fibre attivate da sostanze irritanti ma non dall'attività muscolare
b) fibre attivate dall'attività muscolare ma non da sostanze irritanti
c) fibre attivate dall'attività muscolare e da sostanze irritanti.
Le fibre che conducono a velocità superiore ai 30 m/s probabilmente sono dedicate ai recettori corpuscolari come i fusi muscolari, gli organi tendinei di Golgi, ai corpuscoli di Pacini e Pacini-simili. Non ci sono evidenze scientifiche che queste fibre siano coinvolte nel dolore muscolare.
A livello del corno posteriore del midollo ci sono due tipi di neuroni che rispondono in seguito ad uno stimolo cutaneo, essi sono concentrati a livello della lamina I e delle lamine V e VI. Questi 2 tipi di neuroni nocicettori sono i Neuroni ad Ampio Range di Azione o WDR (Wide Dynamic Range) che possono essere eccitati da stimoli innocui ma che rispondono anche a stimoli di maggiore intensità e di vario tipo sino a rispondere in una scarica di tipo eccitatorio nocicettivo, e poi ci sono i neuroni nocicettivi specifici (NS) che non rispondono a stimoli non nocicettivi a bassa soglia ma richiedono una certa intensità di stimolo per essere attivati. Molti di questi neuroni nocicettori specifici rispondono rispondono a stimoli termici (50-55 °C) o meccanici (pizzico) e corrispondono a piccoli campi recettoriali cutanei governati da fibre di piccolo diametro di tipo A (Gruppo III) e/o C (Gruppo IV), nel caso dei WDR invece gli impulsi provengono da fibre di grosso diametro al quale convergono campi recettoriali a bassa soglia molto ampi. Un altro neurone LTM che va menzionato, e che si trova nelle lamine III e IV del corno posteriore, è quello che serve alla valutazione di stimoli innocui di tipo tattile.
Questi neuroni sarebbero neuroni in cui convergerebbero, oltre gli stimoli cutanei, anche gli stimoli provenienti dai visceri, articolazioni e muscoli. La convergenza di impulsi sia superficiali che profondi sullo stesso neurone è oggi considerato causa di iperalgesia, che si esprime con una scarsa capacità di localizzazione dello stimolo, e con il riferimento del dolore in strutture profonde come ad es. il muscolo.
Questi neuroni di convergenza sarebbero poi anch'essi sotto il dominio dei sistemi di modulazione discendenti.
Come abbiamo visto le fibre che conducono gli impulsi al midollo hanno due velocita' di conduzione; una, gruppo IV ,con velocita' di 2.5 m/sec , questo gruppo sembra mediare il " tenderness " ed il gruppo III con velocita' tra 2.5 e 30 m/sec, che medierebbe il dolore infiammatorio spontaneo.
Queste fibre terminano nelle corna dorsali midollari , in particolare si è visto che i recettori HTM hanno proiezioni nella Lamina I.
Nelle corna dorsali del midollo spinale sono presenti varie popolazioni di cellule che ricevono impulsi da tessuti profondi compresi i muscoli. Sembra però che alcune di queste cellule rispondono esclusivamente a stimoli provenienti dai muscoli scheletrici. Questi neuroni ricevono una forte inibizione discendente, tanto che nelle cellule convergenti l'impulso profondo è maggiormente inibito da questi centri sopraspinali piu' che da input cutanei alla stessa cellula, questa inibizione inoltre si esplica maggiormente sui recettori HTM che LTM.
Questi neuroni sono inoltre sotto il controllo modulatorio delle alterazioni dei loro campi recettoriali , cosicche' la loro sensibilità nella mediazione del dolore profondo non è costante ma soggetta ad influenze modulatorie multicompartimentali.
E' ipotizzabile quindi che sotto varie condizioni patologiche, che alterano i campi recettoriali nella periferia o il sistema inibitorio discendente, l'eccitabilità dei neuroni sia aumentata per lungo tempo.
La forte inibizione discendente sui neuroni convergenti sarebbe anche responsabile della scarsa localizzazione del dolore muscolare, fenomeno quest'ultimo dovuto anche al fatto che le fibre afferenti provenienti da un dato muscolo si distribuiscono a molti segmenti spinali, come avviene per il dolore viscerale.
I fattori periferici che influenzano la sensibilità dei nocicettori muscolari sono vari.
Uno dei principali sintomi soggettivi di alterazione patologica del muscolo scheletrico è il tenderness. Questo fenomeno sembra essere dovuto al fatto che i nocicettori muscolari, che normalmente hanno un'alta soglia di stimolazione meccanica, cambiano le loro proprietà recettive nel tessuto danneggiato e rispondano quindi anche a stimoli meccanici deboli. L'abbassamento della soglia probabilmente è dovuta a sostanze endogene liberate dal muscolo danneggiato.
Le sostanze implicate sono varie e comprendono serotonina, istamina, prostaglandine e neuropeptidi come la calcitonina, la colecistochinina, la sostanza P ed infine la bradichinina la quale sembra agire sui nocicettori del gruppo III . Queste sostanze possono anche potenziarsi nei loro effetti come avviene ad esempio per le prostaglandine PGE2 che potenziano gli effetti stimolanti della bradichinina sul recettore muscolare. Cio' spiegherebbe anche l'azione analgesica dell'ac. acetilsalicilico, che inibendo la sintesi delle PG, abolisce la sensibilizzazione, dei nocicettori indotta dalle PG. Un'ulteriore azione è quella che attraverso il blocco delle cicloossigenasi aumenta il substrato per le lipoossigenasi che sintetizzano grandi quantita di leucotrieni, che sembrano aver un ruolo desensibilizzante a lenta azione sui nocicettori.
L'azione del sistema simpatico sui nocicettori muscolari è di notevole interesse clinico ma ancora in fase di studio. I dati attuali indicano che i recettori non sono influenzati dalla stimolazione simpatica a meno che essi non siano stati sensibilizzati precedentemente da una stimolazione dolorosa. L'adrenalina sembra avere un'azione eccitatoria sui nocicettori meccanici HTM mentre i meccanocettori LTM sono attivati parzialmente e parzialmente depressi da questa amina.
Una lunga ipossia attiva sia i recettori HTM che i LTM.
Il dolore miofasciale primitivo essenziale è una diagnosi relativamente poco conosciuta che evoca l’immagine di un dolore vago, generalizzato, associato a disfunzione. Tuttavia, nonostante una storia di teorie controverse e di una confusa terminologia, il suo inquadramento diagnostico sta diventando clinicamente utile nella classificazione di un’ampia varietà di condizioni dolorose somatiche.
Una chiara diagnosi di dolore miofasciale primitivo essenziale è il passo più importante per il suo trattamento. Può fornire, inoltre, una griglia teorica che aiuta a spiegare un dolore persistente, permettendo l’elaborazione di una strategia terapeutica efficace. Posti di fronte ad un dolore muscolare, infatti, l’obiettivo è:
* evitare di misconoscere un’altra causa di dolore muscolare;
* evitare di misconoscere un dolore miofasciale secondario o coesistente con un’altra manifestazione mialgica.
Nonostante il contributo di Simons, dell’American College of Rheumatology, del Dipartimento di Medicina Fisica e Riabilitativa della Mayo Clinic (che rimangono, comunque, al momento, i riferimenti di ausilio diagnostico più validi) e di altri autorevoli autori, criteri universalmente accettati per la diagnosi del dolore muscolare primitivo essenziale (nelle sue diverse espressioni cliniche) ancora non esistono.
E dal momento che i sintomi di tale condizione clinica sono simili a quelli di uno svariato ventaglio di patologie [Tab.II], si rende necessario, in tutti i casi, un’accurata ricerca di altre cause possibili [Tab.III]. Attualmente, infatti, la diagnosi è prevalentemente di esclusione.
Certamente significativo, anche se non dirimente, è la rilevazione di punti “trigger” o “tender”; e, a proposito, ci sembra utile, rammentare brevemente le caratteristiche fondamentali differenziali tra i 2 tipi di spot mialgici:
|
|
PUNTO TRIGGER |
PUNTO TENDER |
|
Indurimento tessutale (bande tese - taut band) intramuscolare |
Presente |
Assente |
|
Risposta locale di contrazione delle fibre muscolari (local twitch response) |
Presente |
Assente |
|
Dolore riferito in un’area bersaglio (target zone) |
Presente |
Assente |
Uno dei criteri, comunque, che riteniamo più utili in fase differenziale è l’inquadramento in forme cliniche generalizzate o loco-regionali.
In questo ambito il quadro clinico che più di ogni altro pone problemi di differenziazione è la reumoartropatia psicogenica ( e le simulazioni). In tali casi i pazienti riferiscono dolorabilità su quasi ogni area esaminata con palpazione o digitopressione, e, spesso, manifestano una distribuzione delle aree dolorabili che differisce sensibilmente da un’osservazione all’altra.
Di contro, i pazienti affetti da sindrome dolorosa miofasciale (SDM) primitiva essenziale diffusa ( quali la fibromialgia, o la forma diffusa da “tender points”), presentano una dolorabilità elettiva in siti anatomici specifici, che tendono a ripetersi esattamente nelle osservazioni successive [TAB.IV].
I sintomi delle forme diffuse possono essere indistinguibili dalle manifestazioni precoci di altre condizioni reumatologiche (ad es: artrite reumatoide, connettivopatie, spondiloartropatie sieronegative) o di alcune patologie neurologiche (ad es: sclerosi multipla, morbo di Parkinson), oppure essere causati da disturbi metabolici (come l’ipotiroidismo, l’ipoparatiroidismo, l’osteoporosi). In questi casi l’esecuzione di tests di laboratorio quali emocromo, VES, FR, ANA, enzimi muscolari, funzione tiroidea, calcemia, e, specie in presenza di disestesie, parestesie e dolori urenti, un’accurata valutazione neurologica (accompagnata da EMG e studi sulla conduzione nervosa) possono offrire un orientamento diagnostico chiaro. Va sottolineato, inoltre, che il follow-up di quadri non ben definibili, può condurre, con la comparsa di nuovi segni o sintomi, a diagnosi più precise.
Vari quadri clinici ad espressione locale o regionale possono presentare manifestazioni simili alle SDM. La raccolta anamnestica accurata e un attento esame obiettivo possono, comunque, sempre offrire strumenti efficaci di differenziazione. Il dolore di borsiti o tendiniti è sempre abbastanza ben circoscritto, e anche laddove dà luogo a dolore irradiato o riferito, questi non segue mai pattern definiti, a differenza di quello delle SDM che è più sordo, non ben delimitabile, e profondo, e che spesso si estende ad aree di dolore riferito ben codificate.
La polimialgia reumatica deve essere presa in considerazione di fronte a pazienti anziani che lamentano dolori al cingolo scapolare o pelvico. Dirimente è la presenza di valori molto elevati di VES, e una risposta eccezionalmente positiva alla somministrazione di basse dosi di corticosteroidi, completamente inefficaci nelle SDM.
Va sempre valutata attentamente ogni manifestazione neurologica (aree di ipo-anestesia, parestesie, disestesie, iperalgesia, ecc.), per quanto discreta e limitata. La loro presenza, infatti, deve sempre imporre l’esecuzione di tests clinici e strumentali di approfondimento (EMG, studi di conduzione ecc.).
Particolare difficoltà comporta la diagnosi differenziale nei confronti di dolori muscolari dovuti a trigger points in sede non miofasciale (capsule articolari, legamenti, cicatrici). In questi casi, l’intuito, l’esperienza e un’accurata ricerca possono essere gli unici strumenti a disposizione.
Non va mai sottovalutata, inoltre, la possibilità che una SDM insorga in presenza di altra patologia, loco-regionale o diffusa. Ad esempio una condizione dolorosa come l’artrite reumatoide può coesistere con la fibromialgia, oppure una SDM da “trigger points” con un’artropatia.
Il riconoscimento di entrambi i quadri clinici è essenziale per il buon esito del trattamento, dal momento che l’affronto terapeutico di solo una delle due condizioni è spesso seguita da insuccesso e può condurre ad inappropriati accanimenti.
I metodi di trattamento del dolore miofasciale ( nelle sue varie espressioni cliniche e relativi sinonimi) sono numerosi come i terapisti che si cimentano ad affrontarlo. Quadro clinico d’intersezione ( e talvolta di contrapposizione) tra varie specialità, l’apparente varietà di approcci terapeutici possibili denuncia la sostanziale fragilità di ogni specifica modalità, evidenziandone, al di là di ogni opinione, una carenza di provata efficacia.
Come molti interventi in medicina in generale e in algologia in particolare, la strategia terapeutica proposta in questo scritto non è stata oggetto di un rigoroso studio controllato. Si basa, comunque, sull’esperienza elaborata nel nostro ambulatorio di terapia del dolore, orientata sulle linee guida del Dipartimento di Medicina Fisica e Riabilitativa della Mayo Clinic di Rochester.
E’ bene, inoltre, sottolineare che il dolore miofasciale cui faremo riferimento, sia in senso diagnostico differenziale che terapeutico, è quello primitivo essenziale [Tab.I].
Se ad una prima deduzione sembra indispensabile un approccio interdisciplinare, all’analisi clinica questa configurazione si rivela più che la composizione di un puzzle, al completamento del quale ogni specialista, attraverso le proprie metodologie, aggiunge la propria tessera, una frammentazione diagnostica e terapeutica da cui il paziente spesso non trae alcun beneficio.
Nel rispetto, quindi, delle specifiche conoscenze e competenze di ogni settore specialistico, la valutazione del fenomeno dolore, nella sua globalità, richiede la definizione di un ambito clinico proprio (clinica algologica), che abbia come metodologia generale la pianificazione di un procedimento che consenta di gestire il paziente algico programmando uno sviluppo a 4 fasi (metodologia algologica) [Fig.1]:
[1] Analisi clinica (anamnesi, es. obiettivo, tests diagnostici),
[2] Identificazione diagnostica (anche nella sua espressione differenziale),
[3] Soluzione terapeutica (e sue implementazioni),
[4] Revisione valutativa dell’iter diagnostico-terapeutico,
avendo come obiettivo fondamentale quello di fornire al paziente la migliore soluzione analgesica possibile, in accordo con un buon giudizio clinico e psicodinamico.
Non sempre l'obiettivo primario deve essere riferito all'analgesia completa, vuoi perché, in alcuni casi, il paziente può essere improvvisamente disancorato da una struttura circolare di equilibrio, in cui il dolore trovava una sua funzione stabilizzante, vuoi perché, in altri casi, viene perso il significato diagnostico e prognostico del sintomo, vuoi perché, in altri casi ancora, l'unica possibilità sembra relegata al raggiungimento di obiettivi parziali.
Non si può e non si deve prescindere dalla necessità di mettere in atto un procedimento che sappia tener conto delle diverse realtà che impongono scelte e gestioni diverse; va sottolineato, cioè, che la necessità è quella di elaborare una strategia terapeutica adeguata rispetto ai problemi che deve affrontare e non può, quindi, non
a) differenziarsi in interventi di tipo multimodale (attuazione di più tecniche all'interno di una stessa competenza) e/o multidisciplinare (integrazione coordinata di interventi diagnostici e/o terapeutici appartenenti a più competenze);
b) proporsi nell'ottica della minor invasività possibile, della partecipazione del paziente alla terapia, del miglioramento della qualità di vita, del controllo dei disturbi collaterali invalidanti.
Il ricorso ad una strategia terapeutica sottintende, inoltre, una scala di priorità nell'impiego dei mezzi antalgici, e un uso sequenziale preciso delle procedure terapeutiche, che sappiano adattarsi alle specifiche esigenze del singolo paziente, e in cui siano privilegiate, almeno inizialmente, terapie non invasive, farmacologiche e non farmacologiche.
Nell’ambito del trattamento di un quadro clinico così complesso e insidioso com’è quello delle SDM primitive essenziali, è indispensabile, accanto ad una diagnosi ben stabilita, aver chiari i proponimenti essenziali cui tentativamente protendersi, nell’intento assoluto di evitare improvvisazioni, empirismi confusi e l’accanimento terapeutico conseguente a tentativi sovrapposti.
Volendo proporli in modo sintetico, per riprenderli dettagliatamente nelle varie sezioni dedicate alle modalità terapeutiche, possiamo così elencarli:
ò rassicurazione del paziente;
ò riduzione del dolore;
ò promozione del rilassamento muscolare;
ò eliminazione dei fattori di predisposizione e mantenimento;
ò riapprendimento delle normali funzioni neuromuscolari;
ò correzione delle disfunzioni motorie;
ò ripristino di un adeguato livello di forma fisica;
avendo come obiettivi finali quello di:
* fornire al paziente i mezzi per controllare autonomamente i propri disturbi mialgici;
* prevenire la dipendenza o l’abuso del personale sanitario.
Quanto già esposto a proposito dell’elaborazione di una strategia terapeutica differenziata in interventi di tipo multimodale e multidisciplinare[1], trova, nel trattamento delle SDM, la sua collocazione più appropriata.
Come ai più sarà, per esperienza, già ben chiaro, è impensabile affrontare, con successo o almeno con soddisfazione (del paziente), le SDM con l’orientamento, diciamo così, unicista, scegliendo cioè questo o quel trattamento, isolatamente e insistentemente.
Il compito terapeutico, già particolarmente insidioso e difficile, può essere agevolato, a nostro giudizio, solo con un’accorta strategia che sappia integrare più modalità, continuamente rivisitate criticamente alla luce degli obiettivi proposti, evitando una tenacia inutile (dannosa per lo più), e saggiamente ancorati al proponimento di raggiungere un equilibrio, il più soddisfacente possibile, tra tecniche applicate e risultato clinico.
Al momento possiamo individuare gli ambiti in cui orientare l’elaborazione di una strategia efficace, integrandoli tra loro, in:
I.
setting terapeutico
II.
terapia fisica
III.
terapia farmacologica sistemica
IV. supporto psicoterapico
Con il termine “setting terapeutico” vogliamo indicare lo scenario fisico e psicologico all’interno del quale si svolge l’interazione medico-paziente. Vale a dire che le modalità comportamentali e psicologiche di relazione possono essere utilizzate, consapevolmente, come uno strumento terapeutico, al fine di individuare la “via di minor resistenza” attraverso cui rassicurare il paziente e pianificare progetti di rieducazione. In questi pazienti, anzi, possono costituire il passo terapeutico più importante, che ripaga il tempo e gli sforzi investiti.
La rassicurazione del paziente passa attraverso l’informazione che gli si offre circa:
- la propria patologia
¨ chiarendo che è ben conosciuta,
¨ che non ha evolutività maligna,
¨ che, soprattutto, non è una rappresentazione mentale;
- la strategia terapeutica scelta.
È importante, inoltre, stimolare il paziente a recuperare uno stato di indipendenza, rinforzando l’idea di responsabilità e di partecipazione attiva e autonoma, tutto questo attraverso:
¨ la correzione delle abitudini di vita scorrette,
¨ la riduzione degli stress,
¨ l’educazione ad un regime alimentare adeguato e al raggiungimento e/o mantenimento di un peso corporeo appropriato,
¨ la consapevolezza della necessità di acquisire la migliore forma fisica attraverso un programma indipendente di esercizi fisici,
¨ l’automodulazione del dolore.
È evidente che tutto questo non può essere adeguatamente assimilato dalla maggior parte delle persone tramite il solo elencarglielo, occorre, invece, un’opera interattiva, ripetitiva, fatta di continui rinforzi.
Nell’ambito del trattamento delle SDM, la terapia fisica costituisce il capitolo più vasto, e, come tale, più difficilmente componibile in una ordinata ed efficace strategia terapeutica. È quello più specificatamente orientato a trattare disfunzioni miofasciali, siano esse primitive o secondarie, indispensabile e insostituibile per qualunque intervento che voglia pianificare risultati mantenentesi a lungo termine.
Questo approccio conservativo cade in 2 ampie categorie: terapia fisica attiva e terapia fisica passiva [TAB.V], che vanno considerate complementari e inseparabili. Affidarsi, infatti, ad un solo tipo di trattamento provvede spesso solo ad un beneficio temporaneo o, nel peggiore dei casi, ad un’esacerbazione del problema.
Il termine attiva implica lo svolgimento, da parte dl paziente, di attività che sono essenziali per il mantenimento dell’omeostasi corporea. Nessuna tecnica o modalità può, infatti, sostituire il naturale equilibrio corporeo richiesto per una funzione ottimale. Obiettivo principale di questa branca è quello di eliminare i fattori di predisposizione e mantenimento [TAB.VI], nella voce stress meccanici, concorrendo a ridurre il dolore, promovendo il rilassamento muscolare, favorendo il riapprendimento delle normali funzioni neuromuscolari e la correzione delle disfunzioni motorie, e aiutando il paziente a ripristinare un adeguato livello di forma fisica.
La correzione di tali fattori è essenziale per il successo del trattamento e la prevenzione delle ricadute. Nel caso dei cosiddetti stress meccanici, vanno comprese le inadeguatezze strutturali, gli stress posturali, e gli stati di compressione/costrizione muscolare.
Una comune inadeguatezza strutturale è l’asimmetria scheletrica che crea una differenza nella lunghezza degli arti inferiori, asimmetria dovuta ad un arto inf. più corto o ad un’emipelvi più piccola. Sia l’una condizione che l’altra possono spesso perpetuare una SDM: pazienti che accusano un dolore aggravato dalla stazione eretta o dalla deambulazione possono avere una discrepanza di lunghezza, laddove quelli con un’intolleranza alla posizione seduta possono avere una asimmetria pelvica. Un altro stress strutturale è dato dalle disproporzioni quale quella che si evidenzia dal rapporto tra un II metatarso lungo e un I metatarso corto, oppure quella risultante dalla presenza di arti superiori corti in relazione all’altezza del tronco. Anche se si è portati a credere che queste evenienze siano relativamente infrequenti, va sottolineato che vari studi (Rush e Steiner, Beal) riportano una incidenza del problema superiore al 70%.
Oltremodo importante è, anche, l’individuazione e la correzione degli stress posturali quale quelli dovuti a:
A. posture scorrette,
B. prolungati stati di immobilità, specie con il muscolo in posizione accorciata,
C. e, soprattutto, ad abuso muscolare, abuso perpetrato mediante scorretti meccanismi di gestione corporea che rendono i movimenti inutilmente stressanti, le prolungate contrazioni (specie se isometriche), il sovraccarico muscolare dovuto all’esecuzione di movimenti ripetitivi, o a movimenti eccessivamente rapidi e a scatto, o conseguente a sforzi eccessivi,l’ uso eccessivo di uno o più gruppi muscolari.
Nell’ambito delle varie tecniche proposte in tabella, che possono utilmente essere integrate tra loro, ci sembra opportuno offrire qualche chiarimento in più sulla ginnastica posturale Mezieres, non certo perché sia di competenza medica ( va anzi affidata ad esperti e qualificati fisioterapisti), ma perché fornisce del muscolo una interessante prospettiva sia funzionale che terapeutica.
Può definirsi come tecnica di armonizzazione statica globale, alla cui base sono 2 nozioni fondamentali.
La prima è che ciò che chiamiamo “muscolo” è un’unità funzionale di 2 parti differenti, ma funzionalmente inseparabili: gli elementi contrattili, i sarcomeri cioè, inclusi in un sistema elastico, e dall’insieme connettivo-fibroso delle aponeurosi, dei legamenti, dei tendini, ecc.
La seconda è che la muscolatura va distinta in 2 sistemi totalmente differenti, incaricati di 2 funzioni completamente diverse: la muscolatura fasica (o dinamica) e la muscolatura tonica. L’uomo, a differenza di certi quadrupedi, non ha dei muscoli completamente diversificati. Tutti i suoi muscoli sono misti e racchiudono insieme delle unità motorie fasiche e delle unità motorie toniche, e queste sono distribuite in proporzione variabile a seconda della loro funzione.
La muscolatura dinamica è quella che conosciamo meglio. Essa è al servizio del movimento, è una muscolatura rapida che interviene quando lo desideriamo, obbedendo all’azione volontaria. È una muscolatura affaticabile e la sua patologia è la debolezza, il suo trattamento è classico: uno sviluppo in forza che costituisce una parte importante della rieducazione funzionale.
La muscolatura tonica, invece, è una muscolatura lenta, la cui funzione principale è il controllo della statica. Il suo agente meccanico è il riflesso miotattico, il suo sistema di controllo la fusomotricità gamma. È, soprattutto, una muscolatura riflessa, la cui attività sfugge completamente al nostro controllo volontario, né per aumentarla né per diminuirla. La patologia della muscolatura tonica non è mai la debolezza, essendo una muscolatura poco affaticabile, bensì l’accorciamento e la retrazione.
La ginnastica Mezieres è prima di tutto una lotta contro le retrazioni e gli accorciamenti muscolo-connettivali. Nonostante, infatti, tutte queste retrazioni siano locali, a causa del gioco della continuità fasciale, esse si ripercuotono sull’insieme del corpo e la deformità segmentaria o il dolore si localizzano a volte ad un livello più o meno lontano. Per correggere veramente bisogna allungare tutta la catena di tensione, la correzione, cioè, non può essere che globale e deve evitare i compensi. Per far questo dovrà essere progressiva ed essere accompagnata da un rilassamento generale.
Il trattamento Mezieres evolve partendo da uno stiramento muscolo-aponevrotico di tutta la catena di tensione verso un rilassamento globale (fase passiva), quindi passerà ad un riallineamento fisiologico dei segmenti corporei (fase attiva-passiva), per poi evolvere verso un controllo del riallineamento (fase attiva).
In questo contesto il termine “passiva” sta ad indicare che le tecniche di trattamento utilizzate non richiedono la partecipazione attiva del paziente. Sono tutte caratterizzate dall’applicazione di uno stimolo esterno che, però, a seconda della natura di questo, si differenziano in non farmacologica (stimolo fisico) e farmacologica (stimolo chimico).
Scoperta da Kraus e perfezionata da Travell e Simons specificatamente per il trattamento delle SDM, è una tecnica che consente la riduzione del dolore miofasciale (locale o regionale) e il rilassamento muscolare attraverso l’applicazione di uno stimolo cutaneo freddo e l’allungamento passivo dei muscoli coinvolti. La sua indicazione è rivolta esclusivamente a quelle sindromi miofasciali nella cui patogenesi giocano un ruolo fondamentale i punti trigger (TP) o un marcato stato di contrattura o spasmo muscolare. Ha il vantaggio che non richiede una esatta localizzazione dei TP, ma richiede una certa abilità nello svolgere la sequenza in cui si articola la tecnica.
Sequenza che cercheremo di riassumere brevemente, ma esaurientemente in questi passi:
1. il paziente viene posto in posizione comoda e stabile, e invitato a rilassarsi il più possibile,
2. viene, in qualche modo, fissata l’estremità del muscolo coinvolto;
3. a questo punto la cute sovrastante la parte interessata viene irrorata con getti paralleli di liquido raffreddante (Cloruro di etile o Fluorometano), seguendo la lunghezza dei fasci del muscolo coinvolto, in direzione dell’area di dolore riferito;
4. immediatamente dopo l’applicazione del primo stimolo freddo si inizia l’allungamento progressivo del muscolo, continuandolo per tutto il tempo dell’applicazione dello spray;
5. lo spray viene, quindi, irrorato sull’area di dolore riferito collegata a quel muscolo;
6. i passi 3-4-5 vengono ripetuti al più 2 o 3 volte, sino, cioè, al raggiungimento della massima escursione possibile dei movimenti passivi attuabili con il muscolo interessato.
7. La procedura viene, comunque, completata dall’applicazione locale di caldo umido e dall’esecuzione attiva, ripetuta, dei movimenti interessati.
Della tecnica vengono effettuate numerose varianti, alcune utilizzando solo lo stretching, altre solo lo spray, altre ancora lo spray e l’esecuzione dei movimenti attivi, altre infine diversi stimoli ancora. Noi raccomandiamo di utilizzare solo quella o quelle di cui si possiede una rassicurante, efficace esperienza.
Considerata da molti come controparte tecnica dell'agopuntura, l'elettrostimolazione nervosa transcutanea (Transcutaneous Electrical Nerve Stimulation - TENS) è una terapia sintomatica, peraltro non nuova, che ha conquistato un ruolo primario nella medicina moderna, a giudicare dalle migliaia di pazienti sottoposti a questo trattamento per svariate situazioni patologiche che comportano dolore. Dal momento che il metodo è estremamente semplice, non tossico, non invasivo, e, soprattutto, facilmente praticabile anche a domicilio, se ne può prevedere una sempre maggiore diffusione, nonostante alcune perplessità che diversi lavori scientifici manifestano.
Sicuramente va posta un'accurata attenzione diagnostica alla sintomatologia algica da trattare con TENS, tenendo presente che, nell’ambito delle SDM, risentono ben poco di una tale tecnica quelle caratterizzate da dolore diffuso e/o mal localizzato e quelle in corso di trattamento con oppiacei (sic!).
D'altra parte non va dimenticato, però, il vantaggio offerto dai moderni elettrostimolatori, che hanno notevolmente limitato le controindicazioni all’impiego della TENS:
1. pazienti con pace-maker cardiaco;
2. applicazione degli elettrodi sul seno carotideo;
3. alti voltaggi vicino all'aia cardiaca, nei soggetti cardiopatici;
4. nel primo trimestre di gravidanza,
con l'aggiunta di operare con prudenza su pazienti in trattamento con beta-bloccanti.
Nel trattamento delle SDM loco-regionali il valore ottimale dei parametri elettrici è dato da:
FREQUENZA 100Hz
DURATA 50-250 msec.
INTENSITÀ 10-40 mA
ONDA bifasica
Laddove la nostra attenzione terapeutica si rivolga all’applicazione di cicli di TENS è bene aver presente alcune considerazione che ne possono far limitare l’uso.
Infatti:
- possono essere necessarie stimolazioni prolungate e ininterrotte (30’-60’) prima di ottenere sollievo;
- frequentemente si nota una perdita di efficacia nel tempo. Generalmente non più del 30% dei pazienti sottoposti a TENS continua dopo 1 anno;
- è una tecnica apparentemente semplice; in realtà è piuttosto impegnativa sia per il medico, in quanto occorre una scelta accurata dei punti da stimolare e una messa a punto, volta per volta, delle modalità di stimolazione; sia per il paziente, con l’applicazione degli elettrodi ripetuta più volte al giorno per molti mesi.
Di tutte le tecniche non convenzionali è quella che senz'altro gode della maggiore notorietà. Oltre ad una diffusa e consolidata pratica clinica, si avvale del sostegno di un'intensa attività nel campo della ricerca sperimentale e clinica. Non ha certo risolto le perplessità del suo statuto scientifico, ma più di ogni altra pone stimolanti interrogativi, e si configura con un "corpus" che, al di là delle pur enormi difficoltà linguistiche, che certe pessime traduzioni non hanno certo aiutato a superare, offre un esemplare lavoro di sistematizzazione, originale quanto si vuole ma che propone, specie in campo algologico, aspetti di notevole interesse diagnostico e terapeutico. Alla luce, poi, dei moderni concetti di modulazione del dolore, ci è stato possibile rivisitare le ipotesi sui meccanismi d’azione dell’efficacia analgesica dell’agopuntura in una sistemazione più consona alle prospettive scientifiche (Fig.2).
Riconoscendo che l'utilità terapeutica attribuita all'agopuntura si estende ben oltre il campo algologico, in mani esperte può risultare estremamente utile nella terapia delle SDM, sia ad espressione loco-regionale che diffusa. Convinzione, questa, rafforzata dall’osservazione che l’80% dei punti d’agopuntura coincide con punti trigger o tender, e con punti motori.
Se praticata attuando una normale profilassi igienica ed una corretta metodologia di applicazione degli aghi, l'agopuntura non presenta particolari problemi, se si escludono gli, abbastanza rari, episodi lipotimici che possono insorgere durante le primissime sedute di trattamento, dovuti per lo più a tensione emotiva del paziente, e che rispondono facilmente alle più scontate manovre del caso, senza lasciare alcun reliquato. Come controindicazione assoluta presenta l' infissione di aghi in punti del basso addome e della regione lombo-sacrale nelle donne durante i primi tre mesi di gravidanza. Dopo il terzo mese sono, inoltre, controindicati i punti della parte alta dell'addome e quelli che provocano una forte sensazione come Hegu (LI 4), Sanyinjiao (Sp 6), Kunlun (B 60) e Zhiyin (B 67). Non si deve praticare l'agopuntura sulla "fontanella" dei bambini. La letteratura medica cinese del passato fornisce, inoltre, un dettagliato elenco di punti, per lo più situati accanto ad organi vitali o a grandi vasi, che o non vanno mai utilizzati o punti non in profondità.
Come controindicazione
relativa c'è la precauzione da adottare nel trattare pazienti
sovraffaticati, molto deboli o defedati.
Nell’elettroagopuntura (EA) gli aghi infissi vengono collegati ad elettrostimolatori, dedicati, a microcorrenti. In questa modalità, gli schemi di applicazioni subiscono varianti, che gli operatori esperti ben conoscono, anche se rimane ampio spazio alle intuizioni personali, tenendo presente che anche le controindicazioni vengono a modificarsi, avvicinandosi a quelle già esposte a proposito della TENS.
Diverso è anche il meccanismo d’azione dell’EA rispetto a quelli menzionati in riferimento all’agopuntura manuale. Note sono le osservazioni cliniche (riferibili peraltro anche alla TENS) che evidenziano un’azione analgesica naloxone reversibile, mediata (periodo di latenza fino a 20’), di lunga durata, evocata da correnti a bassa frequenza, che sembrano mettere in gioco meccanismi umorali legati ai peptidi opioidi endogeni, a differenza dell’analgesia non antagonizzata dal naloxone, immediata e di breve durata, evocata da correnti ad alta frequenza, che sembrano implicare meccanismi di neuromodulazione.
Meno note le ricerche del Prof. Han Ji-Sheng, uno dei più eminenti studiosi cinesi, direttore del Centro di ricerca per le Neuroscienze dell’Univesità di Pechino e presidente dell’ Associazione cinese per lo studio del dolore. I suoi lavori, condotti con la tecnica della microiniezione anticorpale, hanno evidenziato che gli opioidi endogeni sono coinvolti non solo nell’effetto indotto dalla EA a bassa frequenza, ma anche in quello indotto dalla EA ad alta frequenza.
In particolare, più specificatamente:
· l’analgesia indotta dall’EA a bassa frequenza (2 Hz) implica una mediazione della metaencefalina;
· l’analgesia con EA a media frequenza (15 Hz) è mediata dalla dinorfina B;
· l’analgesia con EA ad alta frequenza (100 Hz) è mediata dalla dinorfina A.
Questo spiegherebbe, tra l’altro, perché l’EA ad alta frequenza risulti naloxone resistente. Infatti, per bloccare l’effetto indotto dall’EA a bassa frequenza è sufficiente una dose di 0.5 mg/Kg di naloxone, mentre per ottenere lo stesso risultato, nel caso di EA ad alta frequenza, è necessario usare una dose massiccia di naloxone (24mg/Kg).
L’applicazione di calore agli strati superficiali corporei attraverso meccanismi di conduzione, convezione e irradiazione è già da tempo ben conosciuta nel trattamento del dolore da patologie muscolo-scheletriche. Sebbene abbia un basso indice di penetrazione corporea, esplicando il massimo della sua efficacia a non oltre 0,5 cm. di profondità, l’apporto di calore superficiale è utilizzato per la sua capacità di ridurre il dolore, per la sua azione decontratturante attraverso la riduzione dell’attività degli efferenti gamma, per l’aumento del range di movimento ottenuto tramite l’aumento dell’estensibilità tessutale, e per l’incremento di flusso circolatorio locale mantenuto per lunghi periodi.
Nell’ambito della terapia delle SDM, e più specificatamente in quelle ad espressione clinica loco-regionale, con una marcata componente di contrattura o spasmo muscolare, o nella cui patogenesi svolgono un ruolo primario i punti trigger, la termoterapia esogena utilizzata è essenzialmente quella che agisce per conduzione, e quindi l’applicazione di caldo-umido (bagni, docce, compresse) locale. Si sfrutta, prevalentemente, la sua azione sedativa sulla tensione muscolare, molto appropriata specie prima di eseguire programmi di allungamento muscolare, anche domiciliari.
È molto indicata anche per prevenire o ridurre la dolenzia muscolare possibile dopo un trattamento iniettivo locale[2]; oppure nelle riacutizzazioni di aree mialgiche precedentemente inattivate, l’applicazione di caldo-umido, insieme al riposo, in molti casi ristabilizza la situazione entro 72 h senza ulteriore terapia.
Il massaggio esprime una tecnica che potremmo definire di manipolazione dei tessuti molli, che, accanto ai benefici di un’azione miorilassante e linfodrenante, provvede ad esercitare una utilissima sensazione di profondo rilassamento psicologico nel soggetto che vi si sottopone.
L’uso del massaggio nel trattamento delle SDM si rivolge, soprattutto, ai quadri clinici di dolore diffuso, in soggetti con spiccata componente tensiva, sia muscolare che psicologica, o comunque incapaci di uscire da un ossessivo autocontrollo, con meccanismi di gestione corporea, quindi, impropri e stressanti.
L’azione analgesica della massoterapia può esplicarsi attraverso numerosi meccanismi, i più significativi dei quali sono: un incremento del flusso circolatorio sottocutaneo e muscolare, per azione sia diretta che riflessa, attraverso la facilitazione delle afferenze cutanee; la stimolazione dei meccanocettori cutanei e di quelli tendinei e fasciali, che provvedono ad esercitare un’azione analgesica e miorilassante.
Il massaggio è soprattutto indicato quando una normale attività muscolare dell’area o aree affette risulta troppo limitata dal dolore, o quando, nel dolore espresso, c’è una componente di origine tendinea o legamentosa. Questi tessuti, infatti, manifestano un’accentuata suscettibilità, spesso esitante in manifestazioni algiche, a motivo della loro attività metabolica ridotta e della relativamente scarsa irrorazione sanguigna. La riduzione dello stress tessutale e l’incremento del flusso circolatorio, con il conseguente incremento di apporti nutritivi e di facilitazione del turn over locale, che il massaggio induce, aiuta senza dubbio ogni altra azione terapeutica associata.
È elettivamente indicata nel trattamento delle SDM da punti trigger, laddove ragioni di inserzione anatomica rendono impossibile un allungamento del muscolo, o quando sono presenti TP non responsivi alla tecnica di stretch and spray.
La sequenza che indichiamo in successione è quella raccomandata da Travell e Simons:
1. a paziente sdraiato, iniettare, con tecnica sterile, nel TP 1-5 ml di Procaina cloridrato 0,5% in soluzione isotonica;
2. subito dopo, allungare passivamente il muscolo con l’aiuto di uno spray raffreddante, con la stessa tecnica descritta in precedenza[3];
3. applicare compresse caldo-umide, per qualche minuto, per ridurre la dolenzia post-iniettiva del muscolo;
4. far compiere al paziente movimenti attivi del muscolo che coprano la completa ampiezza di movimento;
5. se permangono aree mialgiche o restrizione dei movimenti, applicare lo stretch and spray dell’intera unità miotattica, agonisti e antagonisti.
L’ago da impiegare deve essere sempre molto sottile, 22-25 gauge, e comunque più è sottile migliore è l’inattivazione del TP e minore la dolenzia muscolare.
Numerose, inoltre, le varianti che diversi autori immettono nella scelta della soluzione iniettata. Si va dal cosiddetto impiego dell’ago “a secco”, cioè senza somministrazione di alcuna soluzione, all’uso di altri anestetici locali, quali la bupivacaina 0,75% o lidocaina 2%, all’utilizzazione di mélange a base di anestetico locale e ketorolac (60 mg in 60 ml di soluzione).
Rimane nostra ferma convinzione che la migliore scelta è la somministrazione di una soluzione a base di Procaina 0,5% per un insieme di precise considerazioni:
a. tra gli anestetici locali è la più efficace sostanza in grado di provocare una marcata dilatazione arteriolare locale di lunga durata (fino a 24 h);
b. sulla placca motrice produce una curarizzazione parziale che impedisce di sostenere una contrazione prolungata;
c. ha un importante effetto sulla mobilità del Ca++, specie sulla membrana del reticolo sarcoplasmatico e del sarcolemma;
d. tra gli anestetici locali è la sostanza meno miotossica. Ha una minima tossicità sistemica, senza causare irritazione locale. C’è, comunque, da porre attenzione all’aggiunta di adrenalina, che aumenta la necrosi muscolare provocata dagli anestetici locali; essa stessa, da sola, può produrre un’azione lesiva sul muscolo;
e. ha una breve durata d’azione, che risulta essere molto vantaggiosa nel caso di blocchi sensoriali parziali provocati inavvertitamente, in seguito all’iniezione.
La presenza di TP multipli costituisce un limite all’applicazione di questa tecnica; una soluzione può essere l’esecuzione di un blocco del simpatico, utile a ridurre il numero dei TP ad una quantità gestibile.
Vale la pena qui ricordare che la mesoterapia è una metodica terapeutica che fa parte della medicina allopatica, o convenzionale, che consiste, nella sua accezione più rigorosa, nell'effettuare iniezioni intradermiche o sottocutanee superficiali multiple, utilizzando piccole quantità di farmaci della Farmacopea Ufficiale, localmente, nelle zone cutanee corrispondenti alla regione o all'organo leso o doloroso. Entra a far parte delle cosiddette tecniche non convenzionali probabilmente perché non è ancora riuscita a collocarsi in protocolli di strategie terapeutiche, relegando il suo ruolo più conosciuto in un ambito di intervento estetico. La sua efficacia si estende, invece, in modo particolare a quelle patologie in cui le manifestazioni locali sono evidenti, e quando ad essere interessati sono i tessuti di origine mesodermica (sistema scheletrico, muscolare, connettivo mesenchimale, derma e sottocute). In clinica algologica, intervenendo con meccanismi d’azione plurifattoriali (Fig.3), trova particolare indicazione nelle affezioni dolorose a prevalente espressività locale, in special modo in quelle dell'apparato locomotore, sia di natura reumatica che traumatica, e nel trattamento della cefalea. Nella terapia delle SDM è particolarmente utile in quelle a manifestazioni loco-regionali, o multifocali, sia da TP che da punti tender.
Una corretta sterilizzazione degli strumenti eviterà ogni possibilità di infezioni, l'utilizzazione di ago e siringa "a gettar via" cancella ogni problema di sterilizzazione; la formazione di ascessi, poi, è piuttosto appannaggio di iniezioni sottocutanee profonde o intramuscolari. C'è la possibilità di ematomi, in soggetti con fragilità capillare, facilmente ovviabili, reazioni sincopali, non solo conseguenza di una pura reattività emotiva, ma espressione di una reazione anafilattica di tipo I, e reazioni allergiche cutanee, comuni a tutte le introduzioni di farmaco, controllate, comunque, da comune terapia antiallergica, che possono essere contenute con un'accurata anamnesi che faccia escludere i soggetti con diatesi allergica o con reazioni allergiche in atto.
L’utilizzazione dell’intervento mesoterapico, nel trattamento delle SDM, dovrebbe trovare uno spazio sicuramente più ampio di quanto non le sia attualmente concesso. Presenta, infatti, una serie di item che vale la pena non sottovalutare:
* consente l’intervento su aree multiple di patologia, con azioni rapide e di pratica esecuzione;
* è una tecnica a scarsissima invasività, caratteristica che rafforza la compliance del paziente;
* richiede un dosaggio farmacologico estremamente ridotto, con conseguente abbattimento delle reazioni tossiche e collaterali;
* aumenta la durata dell’effetto vasodilatatore della Procaina;
* nel trattamento, infine, dei TP non provoca l’elicitazione della risposta locale di contrazione, e non riacutizza il dolore riferito.
Nel trattamento delle SDM, la terapia farmacologica sistemica svolge un ruolo minore, ritenendo utile ricorre ad essa e, comunque, sempre per periodi relativamente brevi:
- in caso di quadri clinici di dolore diffuso;
- per affrontare crisi dolorose recidivanti o ribelli;
- nella terapia dei disturbi del sonno.
La loro utilizzazione viene, per lo più, riservata alle fasi inziali, come trattamento prodromico, di sostegno a più specifici interventi, specie nel caso debbano essere effettuati programmi di mobilizzazione attiva, che risulta per il paziente accompagnata e limitata dalla sintomatologia dolorosa, oppure laddove si voglia prevenire o ridurre l’eccessiva dolenzia post-trattamento. Nelle SDM questi farmaci sono impiegati per le loro proprietà antalgiche, piuttosto che per quelle antinfiammatorie.
Nella nostra pratica clinica, la prescrizione si indirizza all’uso di:
Ibuprofene-Arginina 400-600 mg x 2-3/die
Naprossene 500 mg x 2/die
Paracetamolo 500 mg x 4/die
L’uso di questi principi attivi, nelle SDM, trova indicazione in quei casi in cui il dolore è refrattario alle terapie specifiche in assenza di identificabili fattori di mantenimento[4], oppure quando il paziente sperimenta un’esagerata dolenzia post-trattamento. È evidente che l’uso sistemico di preparati corticosteroidei va notevolmente limitato, nelle SDM, per il probabile sbilanciamento del rapporto rischio/beneficio a scapito di quest’ultimo. Nel caso sia giudicato utile, preferiamo ricorrere al Prednisone titrando la dose da 60 mg/die fino a 10 mg/die, per poi passare all’uso a giorni alterni.
Diversamente da come ci si potrebbe attendere, nelle SDM l’impiego dei miorilassanti andrebbe riservato alla via topica (mesoterapia). L’uso sistemico è consigliato solo su pazienti selezionati, perché l’effetto decontratturante che ne consegue, va ad ottenersi anche su quei muscoli che stanno provvedendo ad un blocco protettivo, con il risultato di aumentare il carico e, quindi, il dolore sui muscoli affetti.
Il farmaco più indicato è la Ciclobenzaprina, miorilassante strutturalmente correlato ai triciclici, che, alla dose di 10-40 mg al momento di coricarsi, favorisce il sonno e modula l’attività efferente ai fusi muscolari, riducendo così la tensione per via diretta. Può provocare una secchezza delle fauci che, se molto accentuata, richiede la sospensione del trattamento.
L’uso di farmaci antidepressivi sta divenendo sempre più frequente nel trattamento di dolori cronici, incluse le SDM. Generalmente, vengono per lo più utilizzati quelli eterociclici, a motivo della loro più spiccata attività antalgica, attività che sembra essere indipendente dai loro effetti antidepressivi. La risposta analgesica, infatti, si evidenzia più rapidamente e a dosaggi minori rispetto alla risposta antidepressiva, e, al momento, sembra ascrivibile all’azione sui sistemi di neurotrasmissione monaminergica (serotonina, noradrenalina), componenti fondamentali della più importante via inibitoria discendente conosciuta.
Nelle SDM il loro impiego viene utilizzato, però, più che per la loro efficacia analgesica, per ripristinare un ciclo di sonno ristoratore, attraverso la prevenzione dei risvegli precoci e inibendo parzialmente le fasi REM (consentendo, così, un sonno più profondo), e per la loro azione indiretta di miorilassamento.
Le sostanze più comunemente usate sono l’Amitriptilina e la Nortriptilina. La dose iniziale di Amitriptilina, 10-50 mg un’ora prima di coricarsi, può essere aumentata con steps di 25 mg fino a 150-200 mg. Una volta raggiunta la dose terapeutica, la si mantiene per un mese, per poi ridurre gradualmente il dosaggio in un range di 10-150 mg. Se la comparsa di tachicardia, disturbi visivi, o altri effetti anticolinergici, dovessero creare problemi, è bene passare alla Nortriptilina, iniziando con una dose di 10-25 mg, per arrivare fino a 75-100 mg.
Si possono utilizzare, anche in base alla propria esperienza, altri antidepressivi quali la Doxepina, il Trazodone o l’Imipramina, sempre partendo con bassi dosaggi e operando incrementi prudenti. È bene avvisare sempre, e nel modo giusto, il paziente della possibilità di avvertire, al mattino, un senso di stordimento e rallentamento motorio che, nell’arco di una settimana, generalmente scompaiono; così come è utile chiarire che, nel loro caso, sono utilizzati non per la depressione, ma per gli effetti che questi farmaci hanno sul sonno e la muscolatura.
Nonostante l’alta frequenza con cui ansia e/o depressione accompagnano le manifestazioni algiche, specie se croniche, tanto da farle apparire inevitabili compagni di viaggio, cui dedicare riflessioni e attenzioni marginali, e nonostante una non sempre velata resistenza, da parte di alcuni, a desistere dall’intervenire nei delicati equilibri (o squilibri) psicologici del paziente, ci sono situazioni cliniche, specie nell’affronto delle SDM, in cui il supporto psicoterapico, operato da specialisti di formazione medica, si impone come indispensabile. È il caso di pazienti affetti da SDM con marcati stati depressivi e/o ansiosi o che presentano disturbi somatoformi.
Una risposta ansiosa, in pazienti con SDM, è talvolta frutto di diagnosi errate o maldefinite, terapie infruttuose, atteggiamenti, da parte dell’entourage sanitario o affettivo, inadatti. Come tale, può anche essere considerata una fisiologica manifestazione emozionale d’allarme di fronte ad un pericolo.
Così come la diminuzione del tono dell’umore è solo uno dei sintomi della sindrome depressiva, la cui diagnosi prevede il riconoscimento di una serie di altri elementi a carico delle diverse funzioni psichiche. In quanto tale, una deflessione timica può, anch’essa, rappresentare una fisiologica risposta reattiva agli eventi in atto.
Entrambi, però, devono divenire oggetto di attenzione psicoterapica nel momento in cui tendono ad assumere un ruolo primario e clinicamente significativo, nel decorso della patologia dolorosa, tale da assorbire ogni energia reattiva del soggetto.
Diversa è la considerazione nei confronti dei disturbi somatoformi (i disturbi da conversione della vecchia nosografia). In questi casi il problema è una diagnosi differenziale accurata, che consenta di individuare il dolore psicogenico ed affidarlo a specifiche psicoterapie.
Le sindromi dolorose miofasciali primitive essenziali[5]sono espressioni cliniche di frequentissimo riscontro, specie ambulatoriale. Non riescono, però, ad avvalersi di specifiche terapie di comprovata efficacia, e, talvolta, presentano non poche difficoltà diagnostiche.
Crediamo, comunque, che solo un approccio sistematico, una strategia terapeutica, cioè, chiara, flessibile anche se standardizzata, possa produrre l’aspettativa dei migliori risultati possibili.
Nella Fig.4 è rappresentato il diagramma di flusso della condotta sistematica che riteniamo più opportuna:
1. costruire un setting terapeutico idoneo per un rapporto di reciproca, chiara comunicazione[6].
2. Individuare e correggere i fattori di predisposizione e mantenimento[7].
3. Prescrivere sempre un programma di terapia fisica attiva[8].
4. Affrontare con protocolli adeguati il dolore loco-regionale o diffuso.
5. Essere accurati nel ripristinare un ciclo di sonno normale.
6. Stabilire dei programmi che sappiano affrontare adeguatamente la tensione psicologica che, in questi casi, è sempre variamente presente.
7. Monitorizzare i risultati clinici, nell’ottica di una rivalutazione critica nel caso di esiti insoddisfacenti, o di indirizzo a programmi domiciliari e follow-up frequenti laddove la strategia risultasse efficace.
1. Airaksinen, O., and Pontinen, P.J.:
Effects of the electrical stimulation of myofascial trigger points with tension
headache. Acupunct. Electrother. Res., 17/4:285-90, 1992.
2. Ashburn, M.A., and Fine, P.G.:
Evaluation and treatment of chronic pain syndromes. Compr. Ther., 16/2:37-42,
1990.
3. Bannerman, R. H.: Acupuncture: the
WHO view. World Health (Dec.): 24-29, 1979.
4. Bennet, R.M.: Fibromyalgia and the
facts: Sense or nonsense. Rheum. Dis. Clin. North Am., 19/1:45-59, 1993.
5.
Boureau,
F., Luu, M. and Kisielnicki, E.:
Effects of transcutaneous
nerve stimulation (TNS), electrotherapy (ET) , electroacupuncture (EA) on
chronic pain: a comparative study. Pain (suppl. I): 277, 1981.
6. Butler, S.: Present status of
tricyclic antidepressants in chronic pain therapy. In Recent Advances in the Management of Pain: Advances in Pain Research
and Therapy. Benedetti, C., Chapman, C.R., and Moricca, G., eds, 7th ed.,
pp. 173-97, Raven Press, New York, 1984.
7. Calodney, A., Schwarzbach, J., and
Lorren, T.: Characteristics, Pathogenesis, and Management of Myofascial Pain
Syndromes. In Current review of Pain,
Raj, P.P., (Ed), pp.141-154, Current Medicine, Philadelphia, 1994.
8. Cheng, R.S.S., and Pomeranz, B.:
Electrotherapy of chronic musculoskeletal pain: Comparison of electroacupunture
and acupuncture-like transcutaneous electrical nerve stimulation. Clin. J.
Pain, 2/3:143-49, 1986.
9. Citera, J.A.: The use of local
anesthetics in the treatment of chronic pain. Orthop. Nurs., 11/1:27-33, 1992.
10.Culling, R.D., and Kilbourn, L.G.:
Myofascial Pain Syndromes. In Decision
Making in Pain Management, Ramamurthy, S., and Rogers, R., eds., pp.46-7,
Mosby-Year Book, St. Louis, 1993.
11.Fox, E.J. and Melzack, R.:
Transcutaneous electrical stimulation and acupuncture: comparison of treatment
for low-back pain. Pain 2:141-8, 1976.
12.Frampton,
V.M.: A pilot study to evaluate myofascial or trigger point electro-acupuncture
in the treatment of neck and back pain. Physiotherapy., 71/1:5-7, 1985.
13.Gerwin,
R.D.: The management of Myofascial Pain Syndromes. J. Musculoskelet. Pain,
1/3-4:83-94, 1993.
14.Graff-Radford,
S.B., Reeves, J.L., Baker, R.L., and Chiu, D.: Effects of transcutaneous
electrical nerve stimulation on myofascial pain and trigger point sensitivity.
Pain, 37/1:1-5, 1989.
15.Han,
J.: I meccanismi d’azione dell’analgesia con agopuntura. In Orientamenti MTC, 3/3:208-23, Paracelso
Ed., Roma, 1986.
16.Henriksson,
K.G.: Muscle pain in neuromuscular disorders and primary fibromyalgia. Eur. J.
Appl. Physiol, 57:348-52, 1988.
17.Hong,
C.Z.: Lidocaine injection versus dry needling to myofascial trigger point. The
importance of the local twitch response. Am. J. Phys. Med. Rehabil.,
73/4:256-63, 1994.
18.International
Association for the Study of Pain: Management of acute pain: a practical guide.
Ready, L.B., and Edwards, W.T., eds., p. 43, IASP Publications, Seattle, 1992.
19.Jacobs,
M.: Massage for the relief of pain: anatomical and physiological consideration.
Phys. Ther. Rev., 40:96-7, 1960.
20.Jacobsen,
S., Petersen, I.S., and Danneskiold-Samsøe, B.: Clinical features in patients
with chronic muscle pain - with special reference to fibromyalgia. Scand. J.
Rheumatol., 22/2:69-76, 1993.
21.Junnila,
S.Y.T.: Log-term treatment of chronic pain with acupuncture. Part I. Acupunct.
Electro. Ther. Res. Int. J., 12/1:23-36, 1987.
22.Kine,
G.D., and Warfield, C.A.: Myofascial Pain Syndrome. Hosp. Pract.,
21/9:194B-196, 1986.
23.King,
J.C., and Goddard, M.J.: Pain rehabilitation. 2. Chronic pain syndrome and
myofascial pain. Arch. Phys. Med. Rehabil., 75/5, Suppl. (S9-S14), 1994.
24.Knott,
M., and Voss, D.E.: Proprioceptive Neuromuscolar Facilitation: Patterns and
Techniques. 2nd ed. Philadelphia. Harper and Row, 1968.
25.Kraus,
H.: Muscle pain: Recognizing the four primary types. Pain Manage., 2/5:232-237,
1989.
26.Kraus,
H., and Fisher, A.A.: Diagnosis and Treatment of Myofascial Pain. The Mount
Sinai J. Med., Vol.58, 3:235-239, 1991.
27.Leisman,
G., DeMann, D., and Altchek, E.M.: Spinal manipulative therapy in the low back
pain patient. Pain Manage., 4/6:8-15, 1991.
28.Lewith, G.T. and Machin, D.: On the
evaluation of the clinical effects of acupuncture. Pain 16:111-127, 1983.
29.Licht,
S.: Therapeutic Heat and Cold. Everly Press. Baltimore, 1965.
30.Ling,
F.W., and Slocumb, J.C.: Use of the trigger point injections in chronic pelvic
pain. Obstet. Gynecol. Clin. North Am., 20/4:809-15, 1993.
31.McClafin,
R.R.: Myofascial pain syndrome.Primary care strategies for early intervention.
Postgrad. Med., 96/2:56-73, 1994.
32.Mense,
S.: Physiology of Nociception in Muscles. In
Advances in Pain Research and Therapy. Fricton, J.R. and Awad, E. eds,
17:67-85, Raven Press, New York, 1990.
33.Michlovitz,
S.: Thermal Agents in Rehabilitation. FA Davis. Philadelphia, 1986.
34.Pistor,
M.: Un defi therapeutique: mésotherapie. Ed. Maloine. Paris,1974
35.Richardson, P.H. and Vincent, C.A.: Acupunture for the treatment of pain: a review of
evaluative research. Pain 24:15, 1986.
36.Romano,
T.J.: The fibromyalgia syndrome. It’s the real thing. Postgrad. Med.,
83/2:231-243, 1988.
37.Romano,
T.J., and Thompson, J.M.: Myofascial Pain Syndromes. Mayo Clin. Proc.,
66/2:219-220, 1991.
38.Rosomoff,
H.L., Fishbain, D.A., Goldberg, M., Santana, R., and Steele-Rosomoff, R.:
Physical findings in patients with chronic intractable benign pain of the neck
and/or back. Pain, 37/3:279-287, 1989.
39.Sessle,
B.J.: Central Nervous System Mechanisms of Muscular Pain. In Advances in Pain Research and Therapy.
Fricton, J.R. and Awad, E. Eds, 17:87-103, Raven Press, New York, 1990.
40.Simons,
D.G.: Muscular pain syndromes. In Advances
in Pain Research and Therapy, Fricton, J.R., (Ed), 17:1-41. Raven Press.
New York, 1990.
41.Simons,
D.G.: Muscle pain syndromes. J. Man. Med., 6:3-23, 1991.
42.Sjolund, B. and Eriksson, M.: The
influence of naloxone on analgesia produced by peripheral conditioning
stimulation. Brain Research 173:
295-301, 1979.
43.Società Italiana di Mesoterapia:
Mesoterapia. In: Corso pratico di base di
Mesoterapia, a cura di
Bartoletti, C.A., Maggiori, S., Ruggieri, F. e Tomaselli, F.. Ed. Salus
Internazionale, Roma, 1982.
44.Sola,
A.E.: Treatment of myofascial pain syndromes. In Advances in Pain Research and Therapy, Vol.7, Benedetti, C., et al.
(Eds), pp. 467-85. Raven Press. New York, 1984.
45.Spadaro
Antonelli, M.A., and Vawter, R.L.: Nonarticular pain syndromes. Differentiating
generalized, regional, and localized disorders. Postgrad. Med., Vol.91,
2:95-104, 1992.
46.Stedwill, J.E.: Fibromyositis. In Decision Making in Pain Management,
Ramamurthy, S., and Rogers, R., eds., pp.70-1, Mosby-Year Book, St. Louis,
1993.
47.Thompson,
J.M.: Tension Myalgia as a Diagnosis at the Mayo Clinic and Its Relationship to
Fibrositis, Fibromyalgia, and Myofascial Pain Syndrome. Mayo Clin. Proc.,
65:1237-1248, 1990.
48.Travell,
J.G.: The Role of Nutritional, Endocrine, and Other Systemic Factors in
Perpetuating Myofascial Pain and Dysfunction. Presented at The Annual Meeting
of The American Academy of Physical Medicine and Rehabilitation, San Francisco,
November, 1992.
49.Travell,
J.G., and Simons, D.G.: Myofascial Pain Dysfunction. The Trigger Point Manual.
Williams & Williams. Baltimore, 1983.
50.Verkimpe-Morelli, N., and Bienfait,
M.: Armonizzazione statica globale. Metodo delle tre squadre. Marrapese
editore, Roma, 1991.
51.Vincent, C.A. and Richardson, P.H.:
The evaluation of therapeutic acupuncture: concepts and methods. Pain 24:1-13,
1986.
52.Willer, J.C., Roby, A. and Le Bars, D.: Psycophysical and electro- physiological approaches to the
pain-relieving effects of
heterotopic nociceptive stimuli. Brain 107:1095, 1984.
53.Wolfe,
F.: Two muscle pain syndromes. Fibromyalgia and the myofascial pain syndrome.
Pain Manage., 3/3:153-164, 1990.
54.Wolfe,
F., Smythe, H.A., Yunus, M.B., et al.: The American College of Rheumatology
1990: criteria for the classification of fibromyalgia. Arthritis Rheum.,
33/2:160-72, 1990.
55.Woolf, S.L.: Neurophysiologic
mechanism in pain modulation: Relevance of electrical nerve stimulation. In: Clinical transcutaneous electrical nerve
stimulation, Mannheimer, J.S., Lampe, G.N. eds., p.41, F.A. Davis,
Philadelphia, 1984.
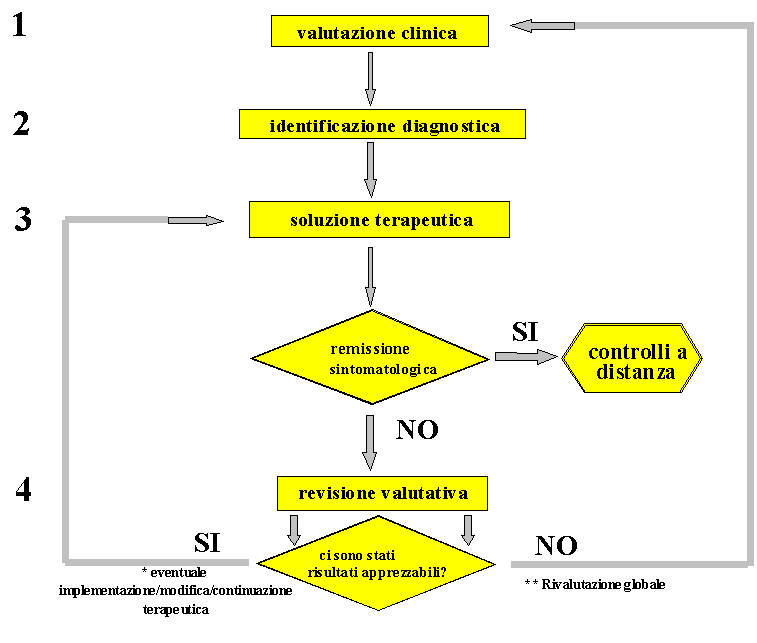 Figura
1. La metogologia algologica: algoritmo decisionale.
Figura
1. La metogologia algologica: algoritmo decisionale.
n MODULAZIONE PERIFERICA
u Modulazione all’input
a) modulazione simpatica periferica
(Santini, Cuello)
b) modificazione delle proprietà di
conduzione delle fibre nervose periferiche (Ignelzi-Nyquist,
Lanza)
u Modificazione del potenziale di placca e desensibilizzazione dei recettoriècorrente di demarcazione
(Lomo, Gunn)
n MODULAZIONE SEGMENTARIA
u Modulazione all’ingresso (“gate control”)
uAttivazione del circuito inibitorio propriospinale (Gebhart e
coll.)
n MODULAZIONE SOPRASEGMENTARIA
u DNIC (Le Bars e coll.)
u Attivazione del “central control trigger”
(Melzack-Casey)
u Attivazione reticolare ( Melzack-Jeans)
u Attivazione talamica (Man-Chen, Chang)
u Attivazione dell’”ansa analgesica mesolimbica”
(Han)
n AZIONE SUI
SISTEMI NEUROCHIMICI DI MODULAZIONE
u Opioidi endogeni (Mayer-Price, Pomeranz, Han,
Sjolund-Terenius-Eriksson)
u Serotonina (Mc Lennan e coll., Han-Terenius)
Figura 2. Ipotesi sui meccanismi d’azione dell'analgesia con agopuntura.
¶ MECCANISMO
REFLESSOTERAPICO
ï
Stimolazione
cutanea
a) Stimolazione
meccanica fasica
b)
Stimolazione meccanica distensiva
- modulazione simpatica periferica
-
corrente di demarcazione
-
circuito inibitorio propriospinale
-
DNIC
· MECCANISMO FARMACOTERAPICO
ï
Modificazioni
tessutali
a) Fase farmacocineticaþ
basse dosi, alti livelli tessutali
di sost.
farmacologicamente attive per un tempo più
lungo.
B) Fase farmacodinamicaþ maggior numero di siti
recettoriali attivati, per minore
escrezione, minor
quantità di farmaco
legato alle proteine plasmatiche,
maggior tempo di
contatto.
Figura 3. Ipotesi sui meccanismi d'azione dell'analgesia con mesoterapia.
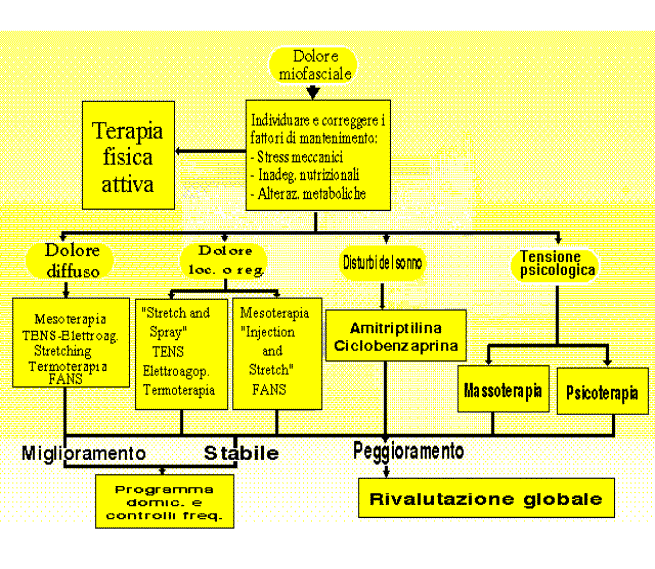
Figura 4. Algoritmo decisionale per il trattamento del dolore muscolare.
ñ TRAUMATICO
ñ MECCANICO
ñ INFIAMMATORIO
ñ RIFERITO
ñ TENDINEO
â PROPRIO
â INSERZIONALE
l
EXTRARTICOLARE
ñ NEUROPATICO
â DA COMPRESSIONE
â DA SINDR. DOLOROSA
REGIONALE
COMPLESSA TIPO I
â SUPERSENSIBILITÀ DA
DENERVAZIONE
ñ MIALGICO
1.
Primitivo
â TRAUMATICO
â INFIAMMATORIO
â METABOLICO
â IATROGENO
â ESSENZIALE
FIBROMIALGIA
SINDR.
DOL. MIOF. DIFFUSA DA Tn.P.
SINDR.
DOL. MIOFASCIALE DA Tr.P.
SINDR.
DOL. MIOFASCIALE DA Tn.P.
2. Secondario
3. Riferito
l
PSICOGENO
ñ DISTURBI
SOMATOFORMI
ñ PAIN
PRONE DISORDERS (SINDR.
DOLOROSA
CRONICA)
ñ PSICOSI
CON ALLUCINAZIONI DI
DOLORE
Tabella I. Classificazione del dolore muscolo-scheletrico. Tn.P.=tender points.
Tr.P.=trigger points.

REUMOARTROPATIE (Stadi precoci)
n DEGENERATIVE
n
INFIAMMATORIE
n
INFETTIVE
n
AUTOIMMUNI
n METABOLICHE
n
EXTRAARTICOLARI
n
PSICOGENE
PATOLOGIE NEUROLOGICHE
n
SCLEROSI MULTIPLA
(Stadio precoce)
n
MALATTIA DI PARKINSON
(Stadio precoce)
n
RADICOLOPATIE
n
NEUROPATIE PERIFERICHE
n
SINDROMI DA
INTRAPPOLAMENTO
SINDR. DOLOROSE DA Tr.P. NON MIOFASCIALI
n
CAPSULE ART.,
LEGAMENTI, CICATRICI
PATOLOGIE INFETTIVE
n
PRODROMI VIRALI,
BATTERICI
n
ENDOCARDITE BATTERICA
SUBACUTA
CHRONIC FATIGUE SYNDROME
PATOLOGIE OSSEE
n
OSTEOPOROSI,
OSTEOMALACIA
n
MORBO DI PAGET
PATOLOGIE ONCOLOGICHE
n
LEUCEMIE ACUTE
n
NEUROMIOPATIA
NEOPLASTICA
PATOLOGIE ENDOCRINOLOGICHE
n
IPOTIROIDISMO
n
IPOPARATIROIDISMO
PATOLOGIE VISCERALI
PATOLOGIE VASCOLARI
Tabella II. Condizioni cliniche da considerare, oltre le SDM primitive essenziali, nella diagnosi differenziale in pazienti con dolore muscolare.

Tabella III. Esami clinici, di laboratorio, strumentali essenziali, utili nella diagnosi in presenza di dolore muscolare.
|
|
SDM da Tr.P. |
Fibromialgia |
Sindr. dolorosa cronica |
|
Analogie |
|
|
|
|
Sintomi |
Dolore muscolare presente Dolore acuto o cronico |
Dolore muscolare presente Dolore cronico |
Dolore muscolare può essere presente o no |
|
Segni |
Dolenzia muscolare alla palpazione |
Dolenzia muscolare alla palpazione |
Dolenzia muscolare alla palpazione può essere presente o no |
|
Differenze |
|
|
|
|
Sintomi |
Distribuzione prevalente locale o regionale del dolore Esordio acuto Occasionalmente presenti anche sintomi non muscolari |
Dolore diffuso Esordio insidioso Usualmente presenti sintomi non muscolari |
Dolore a distribuzione molto variabile, spesso con slittamento della sede nel tempo Esordio insidioso, può seguire una patologia o un trauma acuto Usualmente presenti sintomi non muscolari |
|
Segni |
Punti trigger con tipiche aree di dolore riferito Risposta locale di contrazione presente |
Punti tender senza dolore riferito in ³ 11 dei 18 siti specifici Risposta locale di contrazione assente |
Punti trigger e/o tender possono essere presenti, ma non necessari per la diagnosi Risposta locale di contrazione presente, solo se c’è SDM da Tr.P. |
|
Inabilità |
Minima e temporanea, sotto trattamento |
Spesso parziale, presente o no |
Solitamente completa, con severo scadimento delle condizioni fisiche |
Tabella IV. Diagnosi differenziale schematica tra le espressioni cliniche paradigmatiche delle sindromi dolorose miofasciali (SDM), la sindrome dolorosa miofasciale da punti trigger (Tr.P.), la fibromialgia e un classico disturbo psicogeno, la sindrome dolorosa cronica.
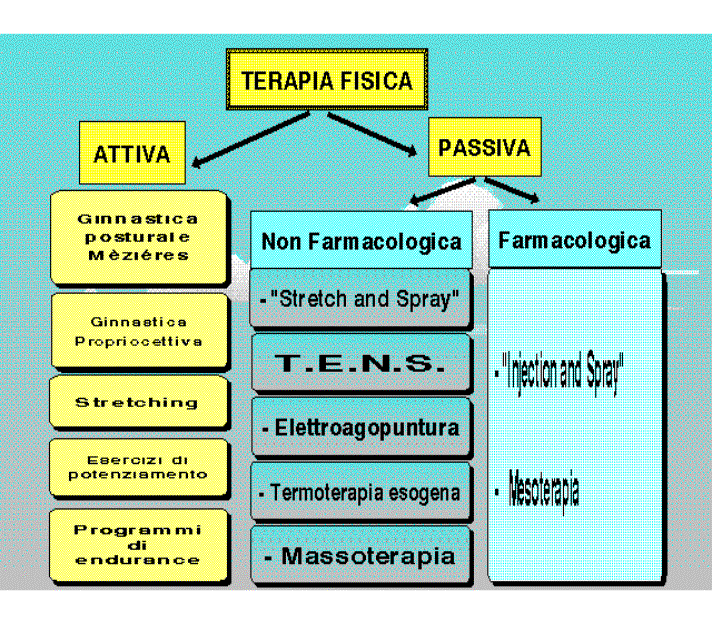
Tabella V. Elenco delle metodiche di terapia fisica più indicate nel trattamento
delle SDM.

Tabella VI. Elenco dei fattori, detti di predisposizione e mantenimento, in grado di
influenzare significativamente il risultato, nella terapia delle SDM.
|
FIBRE |
INNERVAZIONE |
Ø Medio µm
(Range) |
Velocità di conduzione media m/s
(Range) |
|
|
Classificazione di Erlanger/Gasser (Fibre
Afferenti ed Efferenti) |
|
|||
|
A alfa |
Propriocezione, Eff. motori ai muscoli scheletrici |
15 (12-20) |
100 (70-120) |
|
|
ß |
Tatto e afferenti di pressione |
8 (5-15) |
50 (30-70) |
|
|
gamma |
Eff. motori ai fusi muscolari |
6 (6-8) |
20 (15-30) |
|
|
delta |
Meccanotermocettori e nocicettori |
<3 (1-3) |
7 (3-15) |
|
|
B |
Fibre simpatiche pre-gangliari |
3 (1-3) |
7 (3-15) |
|
|
C |
Meccanocettori, Nocicettori, Fibre simpatiche post-gangliari |
1 (0.5-1.5) |
1 (0.5-2) |
|
|
Classificazione di Loyd/Hunt (Solo per le
fibre afferenti muscolari) |
|
|||
|
I a |
Terminazioni spirali e anulari dei fusi neuromuscolari |
13 (11-20) |
75 (70-120) |
|
|
b |
Fusi neurotendinei di Golgi |
|
|
|
|
II |
Terminazioni arboreggianti dei fusi neuromuscolari; tatto, pressione |
9 (4-12) |
55 (25-70) |
|
|
III |
Nocicettori muscolari di pressione, temperatura |
3 (1-4) |
11 (10-25) |
|
|
IV |
Fibre amieliniche C, nocicettori meccanici |
1 (0.5-1.5) |
1 (0.5-2) |
|
Tabella VII. Classificazione delle fibre che innervano il muscolo.
![]() ©Copyright Progetto Salute
©Copyright Progetto Salute